Vienas iš daugelio fizikinių ir cheminių procesų, plačiai pritaikytų tiek pramonėje, tiek kasdieniame gyvenime, yra elektrolizė - elektrodų, prijungtų prie srovės šaltinio, įdėto į tirpalą ar lydalo, jų komponentų (gryno metalo - aliuminio, varis, dujos ir kt.). Pagrindinis įrenginys, kurio viduje vyksta šis procesas, yra elektrolizatorius.

Elektrolizeris
Kas yra elektrolizeris
Elektrolizatorius yra specialus įrenginys, naudojamas jo komponentams atskirti nuo tirpalo ar lydalo.
Pagrindinės elektrolizerio savybės yra šios:
- Vieno elektrodo darbinė įtampa svyruoja nuo 1,8 iki 2,0 V;
- Srovės stipris - normaliam elektrolizės eigai į elektrodus tiekiama srovė, kurios šios charakteristikos vertė yra nuo 5 iki 10 A;
- Elektrodų skaičius - mažiausias elektrodų skaičius yra 2, maksimalų riboja pačios instaliacijos dydis ir jo paskirtis;
- Elektrodų matmenys - kaip elektrodai naudojami ne angliniai strypai, o metalinės plokštės, kurių dydį lemia montavimo tikslas, į plokštes tiekiamos srovės srovės įtampos charakteristika;
- Atstumas tarp priešingai įkrautų elektrodų paviršių - mažiausias atstumas tarp elektrodų plokščių turi būti ne mažesnis kaip 1,5 mm;
- Elektrodo medžiaga - šiuolaikiniuose elektrolizatoriuose nerūdijančio plieno lakštas su nikeliu naudojamas kaip anodo ir katodo medžiaga.
Kita svarbi elektrolizės gamyklos savybė yra katalizatorių naudojimas.
Tokie įrenginiai naudojami šiais tikslais:
- Gauti vandenilio vandenilio dujas, susidedančias iš vandenilio ir deguonies mišinio (Brauno dujos);
- Gryno aliuminio, magnio, cinko išskyrimas iš jų druskos tirpsta;
- Vandens valymas iš druskų ir jame ištirpusių priemaišų;
- Plono nikelio, cinko sluoksnio, apsaugančio nuo korozijos ant metalinių dalių paviršiaus, padengimas;
- Maisto produktų dezinfekavimas;
- Nuotekų valymas iš ištirpusių sunkiųjų metalų ir kitų kenksmingų medžiagų druskų.
Svarbu! Iš paprastos geležies pagamintas platinos elektrodas elektrolizės įmonėse naudojamas rečiau nei iš nerūdijančio plieno, nes jis greičiau oksiduojasi ir tampa nebetinkamas naudoti.
Savarankiškai pagamintas elektrolizatorius
Elektrolizerį savo rankomis gali pasigaminti kiekvienas. Norint surinkti dažniausiai naudojamą dizainą, reikės šių medžiagų:
- nerūdijančio plieno lakštas (geriausi variantai yra užsienio AISI 316L arba mūsų 03X16H15M3);
- varžtai М6х150;
- poveržlės ir veržlės;
- skaidrus vamzdis - galite naudoti gulsčiuką, kuris naudojamas statyboms;
- keletas silkių kaulų jungiamųjų detalių, kurių išorinis skersmuo yra 8 mm;
- plastikinė talpa, kurios tūris 1,5 litro;
- mažas filtras, filtruojantis vandentiekio vandenį, pavyzdžiui, skalbimo mašinų filtras;
- atbulinis vandens vožtuvas.
Surinkimo procesas
Surinkite elektrolizatorių savo rankomis pagal šias instrukcijas:
- Visų pirma reikia pažymėti ir paskesnį nerūdijančio plieno lakšto pjovimą į tapačius kvadratus. Pjauti galima kampiniu šlifuokliu (kampiniu šlifuokliu). Vienas iš tokių kvadratų kampų turi būti nukirstas kampu, kad plokštės būtų tinkamai pritvirtintos;
- Toliau reikia padaryti skylę varžtui plokštės šone, priešingoje kampinio pjūklo pjūviui;
- Plokščių sujungimas turėtų būti atliekamas paeiliui: viena plokštė ant „+“, kita ant „-“ ir pan;
- Tarp skirtingai įkrautų plokščių turėtų būti izoliatorius, kuris veikia kaip vamzdis iš gulsčiuko.Jis turėtų būti supjaustytas žiedais, kurie turėtų būti supjaustyti išilgai, kad gautų 1 mm storio juostas. Šis atstumas tarp plokščių yra pakankamas gerai dujų išsiskyrimui elektrolizės metu;
- Plokštės sujungiamos poveržlėmis taip: ant varžto sėdi poveržlė, tada plokštė, po to trys poveržlės, po plokštės ir pan. Palankiai įkrautos plokštės dedamos į neigiamai įkrautų lakštų veidrodinį vaizdą. Tai leidžia užkirsti kelią pjautinėms briaunoms neliesti elektrodų;


Elektrolizės įrenginio plokštės sumontuotos kartu
- Surinkdami plokštes, tuo pačiu metu turėtumėte jas izoliuoti ir priveržti veržles;
- Be to, kiekviena plokštelė turi būti žieduota, kad įsitikintumėte, jog nėra trumpojo jungimo;
- Be to, visas mazgas turi būti dedamas į plastikinę dėžę;
- Po to verta paryškinti vietas, kur varžtai liečia indo sienas, kur išgręžiate dvi skylutes. Jei varžtai netelpa į konteinerį, tada juos reikia pjauti metaliniu pjūklu;
- Tada varžtai priveržiami veržlėmis ir poveržlėmis, kad konstrukcija būtų sandari;


Plokštės dedamos į plastikinį indą
- Atlikę veiksmus, indo dangtyje turėsite padaryti skylutes ir į jas įkišti jungiamąsias detales. Nepralaidumą šiuo atveju galima užtikrinti sandarinant sandūras sandarikliais silikono pagrindu;
- Apsauginis vožtuvas ir filtras konstrukcijoje yra dujų išleidimo angoje ir tarnauja kaip priemonė kontroliuoti pernelyg didelį dujų kaupimąsi, o tai gali sukelti prastus rezultatus;
- Elektrolizės blokas surenkamas.
Paskutinis etapas yra bandymas, kuris atliekamas panašiai:
- indo pripildymas vandens iki tvirtinimo detalių varžtų žymos;
- maitinimo prijungimas prie prietaiso;
- jungtis su vamzdžio, kurio priešingas galas nuleistas į vandenį, tvirtinimu.
Jei į įrenginį tiekiama silpna srovė, dujų išsiskyrimas per vamzdį bus beveik nepastebimas, tačiau jį bus galima stebėti iš elektrolizatoriaus vidaus. Padidinus kintamąją srovę, į vandenį pridedant šarminį katalizatorių, galima žymiai padidinti dujinės medžiagos išeigą.
Pagamintas elektrolizatorius, kaip taisyklė, yra svarbi daugelio prietaisų, pavyzdžiui, vandenilio degiklio, dalis.


išvaizda vandenilio degiklis, kurio pagrindu laikomas savadarbis elektrolizatorius
Žinodami joninių įrenginių tipus, pagrindines charakteristikas, įtaisą ir veikimo principą, galite teisingai surinkti savo pagamintą konstrukciją, kuri yra puikus asistentas įvairiose kasdienėse situacijose: pradedant suvirinimu ir taupant variklinių transporto priemonių degalų sąnaudas. šildymo sistemų veikimą.
Prietaisas ir veikimo principas
Katodas ir anodas
Paprasčiausias elektrolizės įrenginys susideda iš kelių „elementų“, kurių kiekviena apima:
- 2 plokšteliniai elektrodai - katodas (neigiamas) ir anodas (teigiamas);
- Guminė tarpinė aplink dviejų gretimų nepanašių elektrodų perimetrą.
Išorinėse kamerose yra specialūs vamzdžiai, per kuriuos išleidžiamos išsiskyrusios dujos.
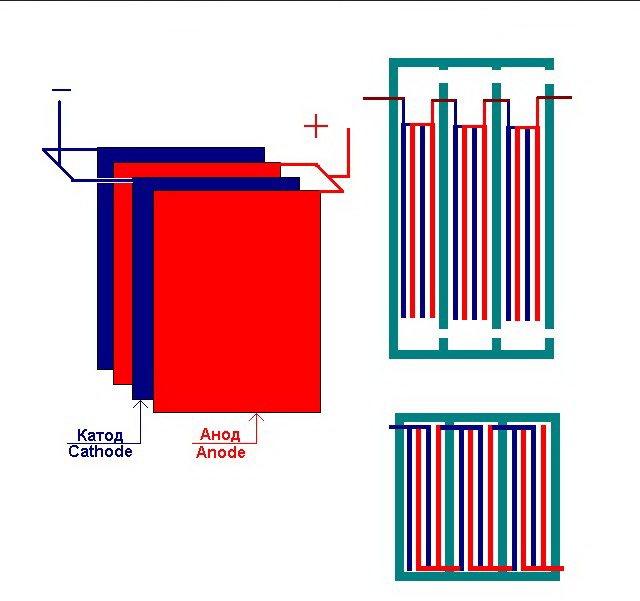

Keletas sujungtų elektrolizės įrenginio „elementų“
Elektrolizeryje gali būti nuo 1 iki 30-40 ar daugiau tokių „elementų“, to paties pavadinimo plokštės sujungtos nuosekliai.
Svarbu! Naudojant maitinimo šaltinius su kintama srove, papildomai naudojami lygintuvai, iš kurių paprasčiausias yra diodinis tiltas.
Toks įrengimas veikia taip:
- Į tarpą tarp elektrodų pilamas distiliuotas vanduo su jame ištirpintu šarmu arba įprasta soda;
- 1,8-2,0 V įtampa tiekiama iš maitinimo šaltinio į visų įrenginio elementų elektrodus;
- Dėl elektrolizės proceso vandenyje ištirpintos medžiagos anijonai (teigiamai įkrauti jonai) pritraukiami prie neigiamai įkrauto katodo, dėl kurio ant jo susidaro plona natrio plėvelė;
- Teigiamai įkrautame anode įvyksta vandens molekulių sunaikinimas, kiekviename susidarant 2 vandenilio atomai ir 1 deguonies atomas;
- Pro atšakos vamzdžius išsiskyrusios detonuojančios dujos patenka į jai skirtą konteinerį.
Elektrolizės proceso intensyvumas priklauso nuo įtampos ir srovės stiprumo - esant žemoms šių charakteristikų vertėms, procesas nebus tęsiamas. Jei maitinimo šaltinis tiekia srovę, kurios srovės įtampos charakteristikos yra per didelės, į elektrolizatorių pilamas tirpalas bus labai karštas ir užvirs.
Derinimas ir įrenginio testavimas
Tada reikia nustatyti, kur varžtai liečia dėžutės sienas, ir tose vietose išgręžti dvi skylutes. Jei be aiškios priežasties paaiškėja, kad varžtai netelpa į konteinerį, tada jie turėtų supjaustykite ir priveržkite veržlėmis, kad būtų sandarūs... Dabar jums reikia išgręžti dangtį ir iš abiejų pusių įdėti sriegines jungtis. Siekiant užtikrinti nepralaidumą, jungtis turėtų būti užplombuota silikono pagrindu.
Savo rankomis surinkę savo elektrolizatorių, turėtumėte jį išbandyti. Norėdami tai padaryti, prijunkite prietaisą prie maitinimo šaltinio, pripildykite jį vandens iki varžtų, uždėkite dangtį, sujungdami vamzdelį su jungtimi ir nuleisdami priešingą vamzdžio galą į vandenį. Jei srovė silpna, srovė bus matoma iš elektrolizatoriaus vidaus.
Palaipsniui didinkite savo namų prietaiso srovę. Distiliuotas vanduo blogai praleidžia elektrą, nes jame nėra druskų ar priemaišų. Norint paruošti elektrolitą, būtina į vandenį įpilti šarmų. Norėdami tai padaryti, turite vartoti natrio hidroksidą (jo yra „Mole“ tipo vamzdžių valytuvuose). Norint išvengti tinkamo dujų kiekio kaupimosi, reikalingas apsauginis vožtuvas.
- Kaip katalizatorių geriau naudoti distiliuotą vandenį ir sodą.
- Dalį kepimo sodos turėtumėte sumaišyti su keturiasdešimt dalių vandens. Šonai iš šonų geriausiai pagaminti iš akrilo stiklo.
- Elektrodai geriausiai pagaminti iš nerūdijančio plieno. Plokštėms tikslinga naudoti auksą.
- Pagrindui naudoti permatomą PVC. Jų dydis gali būti 200–160 milimetrų.
- Maistui gaminti galite naudoti savo pačių pagamintą elektrolizatorių, skirtą visiškam benzino degimui automobiliuose ir daugeliu atvejų.
Sausieji elektrolizatoriai daugiausia naudojami mašinoms. Generatorius padidina degimo variklio galią. Vandenilis užsidega daug greičiau nei skystas kuras, padidindamas stūmoklio jėgą. Be molio, galite vartoti „Mister Muscle“, kaustinę sodą, soda.
Generatorius neveikia geriant vandenį. Geriau prijungti elektrą taip: pirmoji ir paskutinė plokštės - minusas, o ant plokštelės viduryje - pliusas. Kuo didesnis plokščių plotas ir stipresnė srovė, tuo daugiau dujų išsiskiria.
Elektrolizatorių tipai
DIY taškinis suvirinimas baterijoms
Priklausomai nuo konstrukcijos ir veikimo principo, yra 5 elektrolizės įrenginių tipai.
Sausas
Šie elektrolizatoriai susideda iš plokščių elektrodų, atskirtų sandariomis guminėmis tarpinėmis. Dažnai įrenginio „ląstelės“ papildomai dedamos į sandarų gaubtą.
Vandenilis ir deguonis, susidarantys dėl elektrolizės, pašalinami specialiais šakotais vamzdžiais, esančiais korpuso gale arba kraštutinėse įrenginio plokštėse.
Teka
Šio tipo elektrolizės įrenginiuose yra šis įtaisas:
- Elektrolizės vonia (korpusas) su dviem purkštukais, pro kuriuos vienas į ją įleidžiamas elektrolitu, per antrąjį išleidžiamos detonuojančios dujos, susidariusios dėl elektrolizės;
- Plokšteliniai elektrodai, atskirti tarpikliais;
- Talpykla su elektrolitu, esanti virš korpuso su elektrodais ir sujungta žarnomis su įrenginio elektrolizės vonios atšakiniais vamzdžiais ir turinti šakotąjį vamzdį su dujų vožtuvu viršutinėje dalyje.
Veikiant tokiam įtaisui, išsišakojusios dujos per atšakos vamzdį ir žarna patenka į baką su elektrolitu ir, sukurdamos jame tam tikrą slėgį, palieka įrenginį per atšakos vamzdžio vožtuvą.
Membrana
Tokių įrenginių elektrolizės elementai susideda iš dviejų elektrodų, atskirtų plona membrana, kuri leidžia elektrolizės produktams praeiti ir atskiria elektrodus vienas nuo kito.
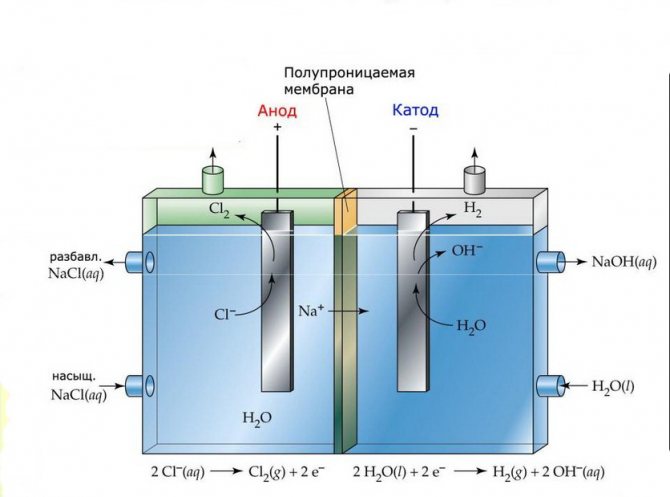

Membraninė elektrolizės gamykla
Diafragma
Tokio tipo elektrolizės įrenginiai susideda iš „U“ formos kolbos, į kurią įkišti du elektrodai, ir 2–3 nepralaidžios diafragmos. Panašūs elektrolizatoriai naudojami atskirai gryno vandenilio ir deguonies gamybai.
Šarminis
Skirtingai nuo kitų elektrolizatorių modelių, juose šarminis tirpalas naudojamas kaip elektrolitas - kaustinė soda (natrio hidroksidas), kuris yra ne tik papildomas vandenilio ir deguonies šaltinis, bet ir elektrolizės katalizatorius.
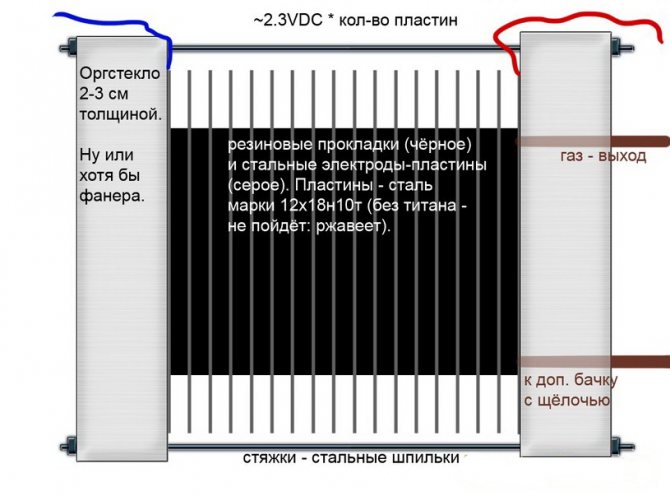

Šarminio elektrolizerio grandinė
Tokie įrenginiai, priešingai nei kitų tipų analogai, leidžia naudoti pigesnius elektrodus iš paprastos geležies.
Atlikite elektrolizatorių savo rankomis
Be abejo, jūs esate susipažinęs su elektrolizės procesu iš pradinės mokyklos programos. Tai yra tada, kai į vandenį po srove dedami 2 poliniai elektrodai, kad gautų gryną metalą ar nemetalą. Elektrolizatorius reikalingas vandens molekulėms suskaidyti į deguonį ir vandenilį. Elektrolizeris, kaip mokslinių mechanizmų dalis, dalija molekules į jonus.
Yra du šio įrenginio tipai:
- Sausas elektrolizatorius (tai yra visiškai uždara ląstelė);
- Šlapias elektrolizatorius (tai yra dvi metalinės plokštelės, dedamos į vandens indą).
Šis prietaisas yra paprastas prietaiso požiūriu, o tai leidžia naudoti net namuose... Elektrolizatoriai dalija molekulių atomų elektrolizės krūvius į krūvio atomus.
Mūsų atveju jis padalija vandenį į teigiamą vandenilį ir neigiamą deguonį. Norėdami tai padaryti, reikalingas didelis energijos kiekis, o norint pagaminti mažiau reikalingo energijos kiekio, naudojamas katalizatorius.
Elektrolizeris vandenilio gamybai
Įžeminimo skaičiavimas
Norėdami savo rankomis surinkti paprasčiausią elektrolizatorių, galite naudoti paveikslėlyje parodytą piešinį.
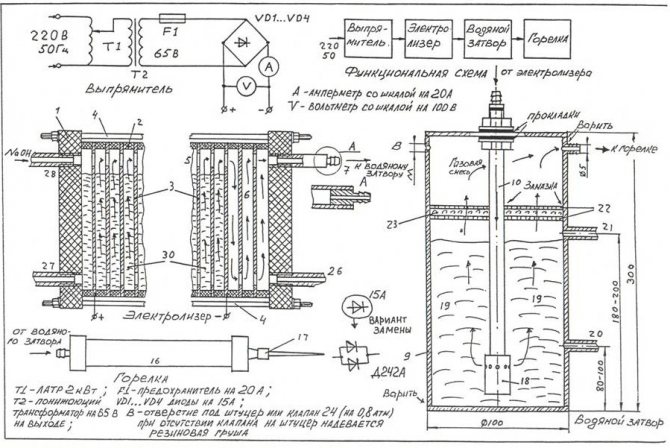

Paprasčiausio naminio elektrolizatoriaus brėžinys
Atkreipkite dėmesį! Elektrolizatorius yra gana pavojingas įrenginys, kuris eksploatacijos metu oksihidrogeninės dujos, susikaupusios dideliais kiekiais, gali sukelti rimtą sprogimą. Įrenginio negalima statyti šalia atviros ugnies šaltinių, šildymo prietaisų.
Pasidaryk pats elektrolizeris automobiliui
Norint pagerinti kuro degimą automobilio variklyje, dažnai surenkamas elektrolizeris, kurį sudaro korpusas iš senos baterijos su viduje įmontuotomis nerūdijančio plieno plokštelėmis, du purkštukai, vienas iš jų sujungtas su bakeliu, užpildytu elektrolitu, antrasis yra prijungtas prie oro tiekimo žarnos prie variklio (tiksliau, su gofruotu nuo oro įleidimo angos iki oro filtro).
Toks naminis tekantis elektrolizeris maitinamas iš automobilio akumuliatoriaus, naudojant relę ir 10 A saugiklį.
Savo rankomis kuriame prietaisą
Šio proceso prietaisą galima atlikti rankomis.
Tam jums reikės:
- Nerūdijančio plieno lakštai;
- Varžtai M6 x 150;
- Poveržlės;
- Riešutai;
- Skaidrus vamzdelis;
- Jungiamieji elementai su sriegiu iš abiejų pusių;
- Pusantro litro plastikinė talpykla;
- Vandens filtras;
- Atbulinis vožtuvas vandens.
Puikus variantas nerūdijančiam plienui yra AISI 316L iš užsienio gamintojo arba 03X16H15M3 iš mūsų šalies gamintojo. Visiškai nereikia pirkti nerūdijančio plieno, galite pasiimti seną. Jums pakanka 50–50 centimetrų.
- Kodėl verta paimti nerūdijantį plieną? - Jūs klausiate. Kadangi labiausiai paplitęs metalas korozijos. Nerūdijantis plienas geriau toleruoja šarmus. Turėtų apklijuokite lapą taip, kad padalytumėte jį į 16 panašių kvadratų... Galite jį supjaustyti kampiniu šlifuokliu. Kiekviename kvadrate supjaustykite vieną iš kampų.
Iš kitos pusės ir priešingo kampo, nuo nupjauto kampo, išgręžkite skylę varžtui, kuris padės suimti plokštes. Elektrolizatorius nenustoja veikti taip:t plokštelės elektra teka į plokštelę - ir vanduo skyla į deguonį ir vandenilį. Dėl to mums reikia geros ir neigiamos plokštelės.
Plokštės turi būti sujungtos pakaitomis: plius minus plius minus, taikant panašų metodą, bus stipri srovė. Norint izoliuoti plokštes iš vienos, naudojamas vamzdis. Žiedas nukerpamas nuo lygio. Ją pjaunant gauname milimetro storio juostelę. Šis atstumas teisingesnis gaminant dujas.
Plokštės yra sujungtos poveržlėmis: ant varžto uždėjome poveržlę, tada plokštę ir tris poveržles, tada vėl plokštę ir pan. Ant pliuso ir minuso reikia pasodinti aštuonias lėkštes. Jei viskas bus padaryta teisingai, tada plokščių pjūviai nelies elektrodų.
Tada reikia priveržti veržles ir izoliuoti plokštes. Tada mes dedame struktūrą į plastikinį indą.
Elektrolizatorių gamintojų apžvalga
Pagrindiniai elektrolizerių gamintojai yra tiek vietinės įmonės („RUSAL“, „NPF RutTech“, UAB „Uralkhimmash“), tiek jų užsienio konkurentai - „Teledyne Energy Systems, Inc“ (JAV), „Hydrogenics Corp.“. (Belgija).
Taigi elektrolizatorius yra gana paprastas ir daug funkcijų turintis įrenginys, naudojamas deginti vandenilio vandenilį, kurį ateityje planuojama naudoti kaip vidaus degimo variklių ir šildymo katilų kurą.
Pasidaryk pats namų elektrolizė
Kai buvau maža, visada norėjau ką nors padaryti pati, savo rankomis. Tačiau tėvai (ir kiti artimi žmonės) daugeliu atvejų to neleido. Ir aš tada nemačiau (ir iki šiol nematau) nieko blogo, kai maži vaikai nori mokytis ??
Žinoma, rašiau ne šį straipsnį, norėdamas prisiminti vaikystės patirtį norėdamas pradėti savišvietą. Tiesiog netyčia, naršydamas internete, susidūriau su tokiu klausimu. Kažkas mažas bombonešis uždavė klausimus, kaip namuose atlikti elektrolizę. Tiesa, aš jam neatsakiau, nes šis berniukas norėjo elektrolizuoti skausmingai įtartiną mišinį ?? Nusprendžiau, kad iš nuodėmės toliau nesakysiu, leisk man pačiam ieškoti knygų. Bet ne taip seniai, vėl klaidžiodamas forumuose, pamačiau panašų chemijos mokyklos mokytojo klausimą. Sprendžiant iš aprašymo, jo mokykla yra tokia skurdi, kad negali (nenori) įsigyti elektrolizerio už 300 rublių. Mokytojas (kokia problema!) Negalėjo rasti išeities iš padėties. Taigi aš jam padėjau. Tiems, kuriems įdomu tokio pobūdžio naminiai gaminiai, aš paskelbiu šį straipsnį svetainėje.
Tiesą sakant, gamybos procesas ir mūsų padėklų naudojimas yra labai primityvus. Bet pirmiausia pasakysiu apie saugumą, o antroje - apie gamybą. Esmė ta, kad mes kalbame apie demonstracinį elektrolizatorių, o ne apie pramonės gamyklą. Dėl to, siekiant saugumo, bus gerai jį maitinti ne iš tinklo, bet iš AA baterijų arba iš baterijos. Natūralu, kad kuo aukštesnė įtampa, tuo greičiau vyks elektrolizės procesas. Tačiau vizualiam dujų burbuliukų stebėjimui tai yra gana pakanka 6 V, bet 220 jau yra per didelis. pavyzdžiui, esant tokiai įtampai, vanduo užvirs greičiausiai, ir tai nėra labai saugu ... Na, manau, kad jūs supratote įtampą?
Dabar pakalbėkime apie tai, kur ir kokiomis sąlygomis eksperimentuosime. Pirmas dalykas, tai turėtų būti laisva vieta arba gerai vėdinama patalpa. Nors viską dariau bute su uždarytais langais ir nieko panašaus? Antra, eksperimentą geriausia atlikti ant gero stalo. Žodis „geras“ reiškia, kad stalas turi būti stabilus arba geresnis, sunkus, standus ir pritvirtintas prie grindų paviršiaus. Tokiu atveju stalo užtiesalas turi būti atsparus agresyvioms medžiagoms. Beje, tam puikiai tinka plytelės iš plytelės (nors, deja, ne visos). Tokia lentelė pravers ne tik šiai patirčiai. Tačiau aš viską padariau ant paprastos taburetės ?? Trečia, eksperimento metu nereikia judinti maitinimo šaltinio (mano atveju - baterijų). Dėl to, norint patikimumo, geriausia juos nedelsiant padėti ant stalo ir pritvirtinti taip, kad jie nejudėtų. Patikėkite, tai yra patogiau nei reguliariai laikyti rankomis. Aš tiesiog prisirišau savo baterijas elektrine juosta prie pirmo matyto kieto daikto. Ketvirta, patiekalai, kuriuose eksperimentuosime, tegul būna maži. Paprastas stiklas tinka arba šūvio stiklas. Beje, tai yra optimaliausias būdas naudoti akinius namuose, priešingai nei į juos pilama alkoholį tolimesniam naudojimui ...
Na, dabar pereikime prie įrenginio. Tai pateikta paveiksle, bet kol kas trumpai paaiškinsiu, kas ir ką.
Turime paimti paprastą pieštuką ir paprastu peiliu nuimti nuo jo medį ir iš pieštuko gauti visą šviną. Tačiau galite paimti švino iš mechaninio pieštuko. Tačiau vienu metu yra du sunkumai. Pirmasis yra įprastas. Mechaninio pieštuko švinas yra per plonas, mums tai tiesiog netinka vizualiniam eksperimentui. Antrasis sunkumas yra kažkokia nesuprantama dabartinių skalūnų kompozicija. Toks jausmas, kad jie pagaminti ne iš grafito, o iš kažko kito. Apskritai mano patirtis su tokiu „švinu“ nebuvo visiškai sėkminga, net esant 24 V įtampai. Dėl to turėjau išsirinkti gerą sumedėjusį paprastą pieštuką. Gautas grafito strypas mums tarnaus kaip elektrodas. Kaip galite įsivaizduoti, mums reikia dviejų elektrodų. Dėl to einame pasirinkti antrojo pieštuko arba tiesiog sulaužyti esamą lazdelę į dvi dalis. Aš iš tikrųjų tai padariau.
Su bet kokia ranka, kuri ateina po ranka, mes suvyniojame pirmąjį švino elektrodą (su vienu laido galu) ir sujungiame šią laidą su energijos šaltinio minusu (su kitu galu). Tada mes imamės antrojo vadovavimo ir darome tą patį su juo. Tam, remiantis tuo, mums reikia antrojo laido. Bet šiuo atveju mes prijungiame šį laidą prie maitinimo šaltinio pliuso. Jei kyla problemų pritvirtinant trapų grafito strypą prie vielos, galite naudoti po ranka esančius įrankius, tokius kaip juosta ar lipni juosta. Jei nepavyko apvynioti grafito galo pačia viela, o juosta ar izoliacinė juosta nesuteikė glaudaus kontakto, tada pabandykite priklijuoti šviną laidžiu klijais. Jei to neturite, bent jau prijunkite laidą prie vielos siūlu. Nereikia bijoti, siūlas neišdegs nuo tokios įtampos ??
Tiems, kurie nieko nežino apie baterijas ir paprastas jų prijungimo taisykles, aš šiek tiek paaiškinsiu. Piršto tipo baterija sukuria 1,5 V įtampą. Paveikslėlyje turiu dvi panašias baterijas. Be to, jie yra sujungti palaipsniui - vienas po kito, ne lygiagrečiai. Naudojant panašią (nuosekliąją) jungtį, galutinė įtampa bus susumuota iš kiekvienos baterijos įtampos, tai yra, man ji yra 1,5 + 1,5 = 3,0 V. Tai yra mažiau nei anksčiau nurodyti 6 voltai. Bet tingėjau eiti nusipirkti dar kelių baterijų. Principas jums ir taip turi būti aiškus ??
Pradėkime eksperimentą. Pavyzdžiui, apsiribosime vandens elektrolize.Pirma, jis yra labai prieinamas (tikiuosi, kad šio straipsnio skaitytojas negyvena Sacharoje), antra, jis yra nekenksmingas. Be to, aš parodysiu, kaip tuo pačiu prietaisu (elektrolizatoriumi) su ta pačia medžiaga (vandeniu) atlikti du įvairūs patirtis. Manau, kad jūs turite pakankamai fantazijos sugalvoti panašių eksperimentų su kitomis medžiagomis krūva ?? Apskritai vanduo iš čiaupo mums tinka. Bet aš rekomenduoju jo pridėti šiek tiek daugiau ir pasūdyti. Truputi - tai reiškia mažą žiupsnelį, o ne visą desertinį šaukštą. Tai yra svarbu! Gerai išmaišykite druską, kad ištirptų. Taigi vanduo, būdamas grynos dielektrikas, puikiai praleis elektrą. eksperimento pradžioje nuvalykite stalą nuo galimos drėgmės, tada uždėkite maitinimo šaltinį ir stiklinę vandens.
Abu elektrodus, esančius esant įtampai, nuleidžiame į vandenį. Tuo pačiu įsitikinkite, kad į vandenį panardintas tik grafitas, o pati viela neturėtų liesti vandens. Eksperimento pradžia gali būti atidėta. Laikas priklauso nuo daugelio rodiklių: nuo vandens sudėties, laidų kokybės, grafito kokybės ir, žinoma, nuo maitinimo šaltinio įtampos. Mano reakcijos pradžia buvo atidėta porai sekundžių. Deguonis pradeda vystytis ant elektrodo, kuris buvo prijungtas prie baterijų pliuso. Vandenilis išsiskirs ant elektrodo, prijungto prie minuso. Reikėtų pažymėti, kad vandenilio burbuliukų yra daugiau. Aplink vandenyje panardintą grafito dalį prilimpa labai maži burbuliukai. Tada kai kurie burbuliukai pradeda plaukti.
Elektrodas eksperimento pradžioje. Dujinių burbuliukų dar nėra. Vandenilio burbuliukai susidarė ant elektrodo, prijungto prie neigiamo baterijų poliaus
Kokie dar eksperimentai gali būti? Jei jau žaidėte pakankamai su vandeniliu ir deguonimi, mes einame į kitą eksperimentą. Tai įdomiau, ypač namų tyrinėtojams. Įdomu tuo, kad galima ne tik pamatyti, bet ir užuosti. Iš ankstesnės patirties gavome deguonies ir vandenilio, kurie, mano nuomone, nėra labai įspūdingi. Kito eksperimento metu gauname dvi medžiagas (beje, naudingas kasdieniame gyvenime). eksperimento pradžioje sustabdykite ankstesnį eksperimentą ir išdžiovinkite elektrodus. Dabar paimkite valgomąją druską (kurią dažniausiai naudojate virtuvės kambaryje) ir ištirpinkite vandens masėje. Šiuo atveju nemaža suma. Tiesą sakant, tinkamas druskos kiekis yra vienintelis dalykas, dėl kurio antroji patirtis skiriasi nuo pirmosios. Ištirpę druską, galite nedelsdami pakartoti eksperimentą. Dabar vyksta kitokia reakcija. Naudojant gerą elektrodą, dabar išsiskiria ne deguonis, o chloras. Neigiamai vertinant, vandenilis taip pat išsiskiria. Kalbant apie stiklą, kuriame yra druskos tirpalas, po ilgesnės elektrolizės jame lieka natrio hidroksidas. Tai yra žinoma kaustinė soda, šarmai.
Chloras, galėsite jį užuosti. Bet siekiant geriausio efekto, rekomenduoju paimti bent 12 V įtampą. Priešingu atveju galite nejausti aromato. Šarmų (po labai ilgos elektrolizės) buvimą stiklinėje galima patikrinti keliais būdais. Paprasčiausias ir žiauriausias yra įkišti ranką į stiklinę. Etninis ženklas sako, kad jei prasideda deginimo pojūtis, stiklinėje yra šarmų. Protingesnis ir aiškesnis būdas yra lakmuso popierėlis. Jei jūsų mokykla tokia skurdi, kad net negali įsigyti lakmuso, jums padės patogūs rodikliai. Vienas iš jų, kaip sakoma, gali būti lašelis burokėlių sulčių ?? Bet visiškai įmanoma į tirpalą įlašinti šiek tiek riebalų. Kiek žinau, turėtų vykti muilinimas.
Labai smalsiems aprašysiu, kas iš tikrųjų įvyko eksperimentų metu. Pirmojo eksperimento metu, veikiant elektros srovei, įvyko panaši reakcija: 2 H2O >>> 2 H2 + O2 Abi dujos natūraliai plaukia iš vandens į paviršių. Beje, plūduriuojančias dujas galima sulaikyti. Ar galite tai padaryti patys?
Kito eksperimento metu reakcija buvo visiškai kitokia.Tai taip pat inicijavo elektros srovė, tačiau dabar ne tik vanduo, bet ir druska veikė kaip reagentai: 4H2O + 4NaCl >>> 4NaOH + 2H2 + 2Cl2 Turėkite omenyje, kad reakcija turi vykti vandens pertekliuje. Norėdami sužinoti, koks druskos kiekis laikomas didžiausiu, galite jį suskaičiuoti pagal pirmiau pateiktą reakciją. Taip pat galite pagalvoti, kaip patobulinti įrenginį ar kokius kitus eksperimentus galima atlikti. Iš tiesų gali būti, kad natrio hipochloritą galima gauti elektrolizės būdu. Laboratorinėmis sąlygomis daugeliu atvejų jis gaunamas dujinį chlorą praleidžiant per natrio hidroksido tirpalą.