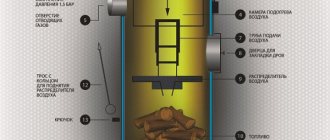
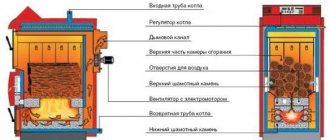
Estabilidad química
Teniendo en cuenta las propiedades químicas de la gasolina, es necesario centrarse en cuánto tiempo permanecerá sin cambios la composición de los hidrocarburos, ya que con un almacenamiento prolongado, los componentes más livianos desaparecen y el rendimiento se reduce en gran medida.
En particular, el problema es agudo si se obtiene un combustible de grado superior (AI 95) a partir de gasolina con un índice de octano mínimo añadiendo propano o metano a su composición. Sus cualidades antidetonantes son superiores a las del isooctano, pero también se disipan instantáneamente.
Según GOST, la composición química del combustible de cualquier marca debe permanecer sin cambios durante 5 años, sujeto a las reglas de almacenamiento. Pero, de hecho, a menudo incluso el combustible recién comprado ya tiene un octanaje por debajo del especificado.
Los vendedores sin escrúpulos son los culpables de esto, que agregan gas licuado a los contenedores con combustible, cuyo tiempo de almacenamiento ha expirado y el contenido no cumple con los requisitos de GOST. Por lo general, se agregan diferentes cantidades de gas al mismo combustible para obtener un octanaje de 92 o 95. La confirmación de tales trucos es el olor acre del gas en la estación de servicio.
Métodos de determinación del punto de inflamación
Existe un método de crisol abierto y cerrado (recipiente para productos derivados del petróleo). Las temperaturas obtenidas difieren debido a la cantidad de vapores acumulados.
El método de crisol abierto incluye:
- Limpiar la gasolina de la humedad con cloruro de sodio.
- Llenar el crisol hasta cierto nivel.
- Calentar el recipiente a una temperatura 10 grados por debajo del resultado esperado.
- Encendido de un quemador de gas sobre la superficie.
- En el momento de la ignición, se registra el punto de inflamación.
El método del crisol cerrado se diferencia en que la gasolina en el recipiente se mezcla constantemente. Cuando se abre la tapa, el fuego se enciende automáticamente.
El aparato de punto de inflamación consta de los siguientes componentes:
- calentador eléctrico (potencia de 600 vatios);
- capacidad de 70 mililitros;
- agitador de cobre;
- encendedor eléctrico o de gas;
- termómetro.
Dependiendo de los resultados, las sustancias inflamables se clasifican:
- especialmente peligroso (en un punto de inflamación por debajo de -200C);
- peligroso (de -200C a + 230C);
- peligroso a temperaturas elevadas (de 230 ° C a 610 ° C).
Velocidad - Combustión - Combustible
¿Cuál es el costo real de 1 litro de gasolina?
La velocidad de combustión del combustible aumenta considerablemente si la mezcla de combustible se encuentra en un intenso movimiento de vórtice (turbulento). Por consiguiente, la intensidad de la transferencia de calor turbulenta puede ser mucho mayor que la de la difusión molecular.
La velocidad de combustión del combustible depende de varias razones que se analizan más adelante en este capítulo y, en particular, de la calidad de la mezcla de combustible con aire. La tasa de combustión de combustible está determinada por la cantidad de combustible quemado por unidad de tiempo.
La tasa de combustión del combustible y, por lo tanto, la tasa de liberación de calor están determinadas por el tamaño de la superficie de combustión. El polvo de carbón con un tamaño máximo de partícula de 300 a 500 micrones tiene una superficie de combustión decenas de miles de veces más grande que el combustible de parrilla de cadena clasificado grueso.
La velocidad de combustión del combustible depende de la temperatura y la presión en la cámara de combustión, aumentando con su aumento. Por lo tanto, después del encendido, la velocidad de combustión aumenta y se vuelve muy alta al final de la cámara de combustión.
La velocidad de combustión del combustible también está influenciada por la velocidad del motor. Con un aumento en el número de revoluciones, se reduce la duración de la fase.
La turbulencia del flujo de gas aumenta bruscamente la velocidad de combustión del combustible debido a un aumento en el área de la superficie de combustión y la velocidad de propagación del frente de llama con un aumento en la velocidad de transferencia de calor.
Cuando funciona con una mezcla pobre, la velocidad de combustión se ralentiza. Por tanto, aumenta la cantidad de calor que desprenden los gases a las piezas y el motor se sobrecalienta. Los signos de una mezcla demasiado pobre son destellos en el carburador y el colector de admisión.
La turbulencia del flujo de gas aumenta bruscamente la velocidad de combustión del combustible debido a un aumento en el área de la superficie de combustión y la velocidad de propagación del frente de llama debido a un aumento en la tasa de transferencia de calor.
Los alcanos normales tienen el número máximo de cetano, que caracteriza la tasa de combustión de combustible en un motor.
La composición de la mezcla de trabajo afecta en gran medida la velocidad de combustión del combustible en el motor. Estas condiciones tienen lugar en coeff.
La influencia de la calidad del desarrollo del proceso de combustión está determinada por la tasa de combustión del combustible en la fase principal. Cuando se quema una gran cantidad de combustible en esta fase, los valores de pz y Tz aumentan, la proporción de combustible postcombustible disminuye durante el proceso de expansión y el índice politrópico nz aumenta. Este desarrollo del proceso es el más favorable, ya que se consigue el mejor aprovechamiento del calor.
En el proceso de trabajo del motor, el valor de la tasa de combustión del combustible es muy importante. Se entiende por tasa de combustión la cantidad (masa) de combustible que reacciona (quema) por unidad de tiempo.
Varios fenómenos generales indican que la velocidad de combustión del combustible en los motores es bastante natural, no aleatoria. Esto se indica por la reproducibilidad de ciclos más o menos inequívocos en el cilindro del motor, lo que, de hecho, determina el funcionamiento estable de los motores. En los mismos motores, la naturaleza prolongada de la combustión siempre se observa con mezclas magras. El trabajo duro del motor, que ocurre a una alta velocidad de reacciones de combustión, se observa, por regla general, en los motores diésel sin compresor, y el trabajo suave, en los motores con encendido por chispa eléctrica. Esto indica que la formación e ignición de mezclas fundamentalmente diferentes provocan un cambio regular en la velocidad de combustión. Con un aumento en el número de revoluciones del motor, la duración de la combustión disminuye con el tiempo y aumenta el ángulo de rotación del cigüeñal. Las curvas cinéticas del curso de combustión en motores son de naturaleza similar a las curvas cinéticas de una serie de reacciones químicas que no están directamente relacionadas con los motores y que ocurren en diferentes condiciones.
Los experimentos indican la dependencia de la intensidad de la transferencia de calor radiante de la velocidad de combustión del combustible. Con una combustión rápida en la base del soplete, se desarrollan temperaturas más altas y se intensifica la transferencia de calor. La falta de homogeneidad del campo de temperatura, junto con las diferentes concentraciones de partículas emisoras, conduce a la falta de homogeneidad del grado de negrura de la llama. Todo lo anterior crea grandes dificultades para la determinación analítica de la temperatura del radiador y el grado de emisividad del horno.
En una llama laminar (consulte la Sección 3 para obtener más detalles), la velocidad de combustión del combustible es constante y Q 0; el proceso de combustión es silencioso. Sin embargo, si la zona de combustión es turbulenta, y este es el caso en consideración, incluso si el consumo de combustible es constante en promedio, la tasa de combustión local cambia con el tiempo y para un elemento de pequeño volumen Q.Q. La turbulencia perturba continuamente la llama; en un momento dado, la combustión está limitada por esta llama o una serie de llamas, ocupando una posición aleatoria en la zona de combustión.
Combustible gaseoso
El combustible gaseoso es una mezcla de varios gases: metano, etileno y otros hidrocarburos, monóxido de carbono, dióxido de carbono o dióxido de carbono, nitrógeno, hidrógeno, sulfuro de hidrógeno, oxígeno y otros gases, así como vapor de agua.
El metano (CH4) es el componente principal de muchos gases naturales. Su contenido en gases naturales alcanza el 93 ... 98%. La combustión de 1 m3 de metano libera ~ 35 800 kJ de calor.
Los combustibles gaseosos también pueden contener pequeñas cantidades de etileno (C2H4). La combustión de 1 m3 de etileno produce ~ 59 000 kJ de calor.
Además de metano y etileno, los combustibles gaseosos también contienen compuestos de hidrocarburos, como propano (C3H8), butano (C4H10), etc. La combustión de estos hidrocarburos produce más calor que la combustión de etileno, pero su cantidad es insignificante en gases combustibles. .
El hidrógeno (H2) es 14,5 veces más ligero que el aire. La combustión de 1 m3 de hidrógeno libera ~ 10800 kJ de calor. Muchos gases combustibles, distintos del gas de horno de coque, contienen cantidades relativamente pequeñas de hidrógeno. En gas de horno de coque, su contenido puede llegar al 50 ... 60%.
El monóxido de carbono (CO) es el principal componente combustible del gas de alto horno. La combustión de 1 m3 de este gas produce ~ 12,770 kJ de calor. Este gas es incoloro, inodoro y muy tóxico.
El sulfuro de hidrógeno (H2S) es un gas pesado con un olor desagradable y muy tóxico. La presencia de sulfuro de hidrógeno en el gas aumenta la corrosión de las partes metálicas del horno y el gasoducto. El efecto nocivo del sulfuro de hidrógeno se ve reforzado por la presencia de oxígeno y humedad en el gas. La combustión de 1 m3 de sulfuro de hidrógeno libera ~ 23 400 kJ de calor.
El resto de gases: CO2, N2, O2 y vapor de agua son componentes de lastre, ya que a medida que aumenta el contenido de estos gases en el combustible, disminuye el contenido de sus componentes combustibles. Su presencia conduce a una disminución de la temperatura de combustión del combustible. Los combustibles gaseosos> 0,5% de oxígeno libre se consideran peligrosos por motivos de seguridad.
Hervir - gasolina
Número de octano Composición de la gasolina
La gasolina comienza a hervir a una temperatura relativamente baja y avanza de manera muy intensa.
No se especifica el final del punto de ebullición de la gasolina.
El inicio de la ebullición de la gasolina es inferior a 40 C, el final es de 180 C, la temperatura de inicio de cristalización no supera los 60 C. La acidez de la gasolina no supera 1 mg / 100 ml.
El punto de ebullición final de la gasolina según GOST es de 185 C, y el real es de 180 C.
El punto de ebullición final de la gasolina es la temperatura a la que una porción estándar (100 ml) de la gasolina probada se destila por completo (se hierve) del matraz de vidrio en el que estaba ubicada en el receptor del refrigerador.
| Esquema de instalación de estabilización. |
El punto de ebullición final de la gasolina no debe superar los 200-225 C.Para las gasolinas de aviación, el punto de ebullición final es mucho menor, llegando en algunos casos hasta 120 C.
MPa, el punto de ebullición de la gasolina es 338 K, su masa molar promedio es 120 kg / kmol y el calor de vaporización es 252 kJ / kg.
El punto de ebullición inicial de la gasolina, por ejemplo 40 para la gasolina de aviación, indica la presencia de fracciones ligeras de bajo punto de ebullición, pero no indica su contenido. El punto de ebullición de la primera fracción del 10%, o temperatura inicial, caracteriza las propiedades iniciales de la gasolina, su volatilidad y la tendencia a formar tapones de gas en el sistema de suministro de gasolina. Cuanto menor es el punto de ebullición de la fracción del 10%, más fácil es arrancar el motor, pero también mayor es la posibilidad de que se formen bloqueos de gas, que pueden provocar interrupciones en el suministro de combustible e incluso parar el motor. El punto de ebullición demasiado alto de la fracción de partida dificulta el arranque del motor a temperaturas ambiente bajas, lo que conduce a pérdidas de gasolina.
| Influencia del punto final del punto de ebullición de la gasolina en su consumo durante el funcionamiento del vehículo. Efecto de la temperatura de destilación del 90% de la gasolina sobre el octanaje de las gasolinas de diversos orígenes. |
Una disminución en el final del punto de ebullición de las gasolinas de reformado conduce a un deterioro de su resistencia a la detonación. Se necesitan investigaciones y cálculos económicos para abordar este problema.Cabe señalar que en la práctica extranjera de varios países, actualmente se están produciendo y utilizando gasolinas de motor con un punto de ebullición de 215 - 220 C.
| Influencia del punto final del punto de ebullición de la gasolina en su consumo durante el funcionamiento del vehículo. Influencia de la temperatura de destilación de la gasolina al 90% en el octanaje de gasolinas de diversos orígenes. |
Una disminución en el final del punto de ebullición de las gasolinas de reformado conduce a un deterioro de su resistencia a la detonación. Se necesitan investigaciones y cálculos económicos para abordar este problema. Cabe señalar que en la práctica extranjera de varios países, actualmente se están produciendo y utilizando gasolinas de motor con un punto de ebullición de 215 - 220 C.
Si el punto de ebullición final de la gasolina es alto, es posible que las fracciones pesadas que contiene no se evaporen y, por lo tanto, no se quemen en el motor, lo que provocará un mayor consumo de combustible.
La reducción del punto de ebullición final de las gasolinas de destilación directa conduce a un aumento de su resistencia a la detonación. Las gasolinas de destilación directa de bajo octanaje tienen un octanaje de 75 y 68, respectivamente, y se utilizan como componentes de las gasolinas de motor.
Combustión - gasolina
Diseño y funcionamiento del sistema de inyección directa de gasolina Bosch Motronic MED 7
La combustión de gasolina, queroseno y otros hidrocarburos líquidos se produce en la fase gaseosa. La combustión puede ocurrir solo cuando la concentración de vapor de combustible en el aire está dentro de ciertos límites, individuales para cada sustancia. Si hay una pequeña cantidad de vapores de combustible en el aire del IB, no se producirá la combustión, así como en el caso de que haya demasiados vapores de combustible y no haya suficiente oxígeno.
| Cambio de temperatura en la superficie del queroseno durante la extinción con espumas. Distribución de temperatura en queroseno antes del inicio de la extinción (ay al final. |
Cuando la gasolina se quema, se sabe que se forma una capa homotérmica, cuyo espesor aumenta con el tiempo.
Cuando la gasolina se quema, se forman agua y dióxido de carbono. ¿Puede esto servir como confirmación suficiente de que la gasolina no es un elemento?
Cuando se queman gasolina, queroseno y otros líquidos en tanques, la fragmentación del flujo de gas en volúmenes separados y la combustión de cada uno de ellos por separado son especialmente visibles.
Cuando se queman gasolina y aceite en tanques de gran diámetro, el carácter del calentamiento difiere significativamente del descrito anteriormente. Cuando se queman, aparece una capa caliente, cuyo grosor aumenta naturalmente con el tiempo y la temperatura es la misma que la temperatura en la superficie del líquido. Debajo de él, la temperatura del líquido desciende rápidamente y se vuelve casi la misma que la temperatura inicial. La naturaleza de las curvas muestra que durante la combustión, la gasolina se descompone en dos capas: una superior y otra inferior.
Por ejemplo, quemar gasolina en el aire se denomina proceso químico. En este caso, se libera energía, equivalente a aproximadamente 1300 kcal por 1 mol de gasolina.
El análisis de los productos de combustión de gasolinas y aceites está adquiriendo una gran importancia, ya que el conocimiento de la composición individual de dichos productos es necesario para el estudio de los procesos de combustión en el motor y para el estudio de la contaminación del aire.
Así, cuando se quema gasolina en tanques anchos, hasta el 40% del calor liberado como resultado de la combustión se consume por radiación.
Mesa 76 muestra la velocidad de combustión de la gasolina con aditivos de tetranitro-metano.
Los experimentos han demostrado que la velocidad de combustión de la gasolina desde la superficie del tanque está significativamente influenciada por su diámetro.
| Alineación de fuerzas y medios al extinguir un incendio en el tramo. |
Con la ayuda del GPS-600, los bomberos hicieron frente con éxito a la eliminación de la quema de gasolina que se derramaba a lo largo de la vía férrea, asegurando el movimiento de los operadores troncales al lugar de acople de tanques.Después de desconectarlos, con un trozo de cable de contacto, conectaron 2 tanques con gasolina al camión de bomberos y los sacaron de la zona de fuego.
| La velocidad de calentamiento de los aceites en tanques de varios diámetros. |
Se notó un aumento particularmente grande en la velocidad de calentamiento debido al viento al quemar gasolina. Cuando se quemaba gasolina en un tanque de 264 ma una velocidad del viento de 13 m / s, la tasa de calentamiento era de 963 mm / min, y a una velocidad del viento de 10 m / s, la tasa de calentamiento aumentó a 17 1 mm / min.
Punto de inflamación y otros parámetros
La combustión del carbón es una reacción química de oxidación del carbono que se produce a una temperatura inicial elevada con una intensa liberación de calor. Ahora es más simple: el combustible de carbón no se puede encender como el papel; se requiere un precalentamiento a 370-700 ° C para el encendido, dependiendo de la marca del combustible.
Momento clave. La eficiencia de la combustión de carbón en un horno o una caldera doméstica de combustible sólido se caracteriza no por la temperatura máxima, sino por la integridad de la combustión. Cada molécula de carbono se combina con dos partículas de oxígeno en el aire para formar dióxido de carbono CO2. El proceso se refleja en la fórmula química.
Si limita la cantidad de oxígeno entrante (cubra el soplador, cambie la caldera TT al modo de combustión lenta), en lugar de CO2, se forma monóxido de carbono gas combustible CO que se emite en la chimenea, la eficiencia de combustión disminuirá significativamente. Para lograr una alta eficiencia, es necesario proporcionar condiciones favorables:
- Las brasas marrones se encienden a una temperatura de +370 ° C, la piedra - 470 ° C, la antracita - 700 grados. Es necesario precalentar la unidad de calefacción con leña (briquetas de aserrín).
- Se suministra aire a la cámara de combustión en exceso, el factor de seguridad es 1.3-1.5.
- La combustión se apoya en la alta temperatura de las brasas que se encuentran sobre la parrilla. Es importante asegurar el paso del oxígeno por todo el espesor del combustible, ya que el aire pasa por el cenicero debido al tiro natural de la chimenea.
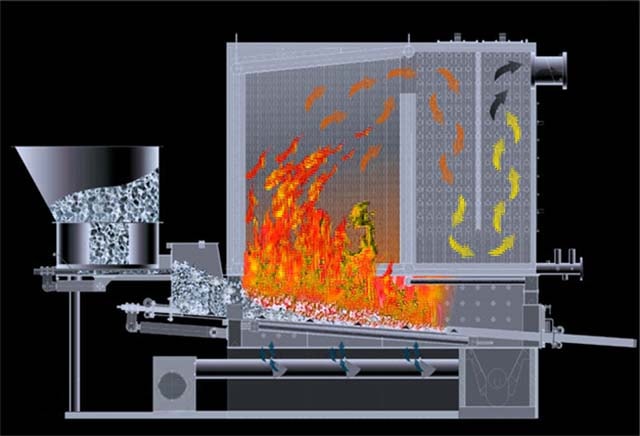
Comentario. Las únicas excepciones son las estufas caseras tipo Bubafonya y las calderas cilíndricas de combustión superior, donde se introduce aire en la cámara de combustión de arriba a abajo.
La temperatura de combustión teórica y la transferencia de calor específica de varios combustibles se muestran en la tabla comparativa. Se nota que, en condiciones ideales, cualquier combustible liberará el máximo calor al interactuar con el volumen de aire requerido.
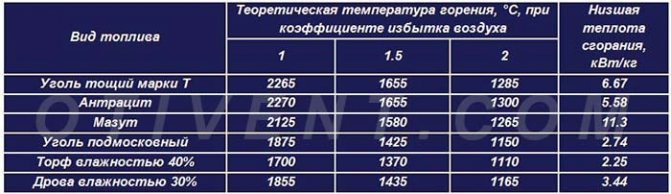

En la práctica, no es realista crear tales condiciones, por lo que el aire se suministra con algo de exceso. La temperatura real de combustión del lignito en una caldera TT convencional está dentro de los 700 ... 800 ° C, piedra y antracita - 800 ... 1100 grados.
Si se excede con la cantidad de oxígeno, la energía comenzará a gastarse en calentar el aire y simplemente volará hacia la tubería, la eficiencia del horno disminuirá notablemente. Además, la temperatura del fuego puede alcanzar los 1500 ° C. El proceso se asemeja a un fuego ordinario: la llama es grande, hay poco calor. En el video se presenta un ejemplo de combustión eficiente de carbón con un quemador de retorta en una caldera automática:
Temperatura - combustión - combustible
| Dependencia del criterio B de la relación entre el área de fuentes de calor y el área del taller. |
La intensidad de la irradiación del trabajador depende de la temperatura de combustión del combustible en el horno, el tamaño del orificio de carga, el grosor de las paredes del horno en el orificio de carga y, finalmente, de la distancia a la que se encuentra el trabajador de la carga. agujero.
| Las relaciones CO / CO y H2 / HO en los productos de combustión incompleta de gas natural, según el coeficiente de consumo de aire a. |
La temperatura prácticamente alcanzable 1L es la temperatura de combustión del combustible en condiciones reales. Al determinar su valor, se tienen en cuenta las pérdidas de calor al medio ambiente, la duración del proceso de combustión, el método de combustión y otros factores.
El exceso de aire afecta drásticamente la temperatura de combustión del combustible.Entonces, por ejemplo, la temperatura real de combustión del gas natural con un 10% de exceso de aire es 1868 C, con un 20% de exceso de 1749 C y con un 100% de exceso de aire, disminuye a 1167 C. Por otro lado , el precalentamiento del aire, que pasa a la combustión del combustible, aumenta la temperatura de su combustión. Entonces, cuando se quema gas natural (1Max 2003 C) con aire calentado a 200 C, la temperatura de combustión aumenta a 2128 C, y cuando el aire se calienta a 400 C, hasta 2257 C.
| Diagrama general del horno. |
Al calentar aire y combustible gaseoso, la temperatura de combustión del combustible aumenta y, en consecuencia, también aumenta la temperatura del espacio de trabajo del horno. En muchos casos, alcanzar las temperaturas requeridas para un proceso tecnológico dado es imposible sin un alto calentamiento del aire y el combustible gaseoso. Por ejemplo, la fundición de acero en hornos de hogar abierto, para la cual la temperatura del soplete (flujo de gases ardientes) en el espacio de fusión debe ser de 1800 a 2000 C, sería imposible sin calentar el aire y el gas a 1000-1200 C. Cuando calentar hornos industriales con combustible local bajo en calorías (leña húmeda, turba, lignito), su trabajo sin calentar el aire es a menudo incluso imposible.
Puede verse en esta fórmula que la temperatura de combustión del combustible se puede aumentar aumentando su numerador y disminuyendo el denominador. La dependencia de la temperatura de combustión de varios gases de la relación de exceso de aire se muestra en la Fig.
El exceso de aire también afecta drásticamente la temperatura de combustión del combustible. Entonces, la salida de calor del gas natural con un exceso de aire del 10% - 1868 C, con un exceso de aire del 20% - 1749 C y con un exceso del 100% es igual a 1167 C.
Si la temperatura de la unión caliente está limitada únicamente por la temperatura de combustión del combustible, el uso de la recuperación permite aumentar la temperatura Тт aumentando la temperatura de los productos de combustión y así aumentar la eficiencia global del TEG.
El enriquecimiento de la explosión con oxígeno conduce a un aumento significativo de la temperatura de combustión del combustible. Como los datos del gráfico en la Fig. 17, la temperatura teórica de combustión del combustible está asociada al enriquecimiento de la explosión con oxígeno por una dependencia, que es prácticamente lineal hasta el contenido de oxígeno en la explosión del 40%. A mayores grados de enriquecimiento, la disociación de los productos de combustión comienza a tener un efecto significativo, como resultado de lo cual las curvas de la dependencia de la temperatura con el grado de enriquecimiento de la explosión se desvían de las líneas rectas y se acercan asintóticamente a las temperaturas limitantes para un determinado Gasolina. Por lo tanto, la dependencia considerada de la temperatura de combustión del combustible del grado de enriquecimiento de oxígeno de la explosión tiene dos regiones: la región de enriquecimientos relativamente bajos, donde hay una dependencia lineal, y la región de enriquecimientos altos (más del 40%), donde el aumento de temperatura tiene un carácter decadente.
Un indicador termotécnico importante del funcionamiento del horno es la temperatura del horno, que depende de la temperatura de combustión del combustible y de la naturaleza del consumo de calor.
La ceniza del combustible, dependiendo de la composición de las impurezas minerales, a la temperatura de combustión del combustible puede fundirse en trozos de escoria. La característica de la ceniza de combustible en función de la temperatura se da en la tabla. PERO.
El valor de tmaK en la tabla. IV - З - temperatura calorimétrica (teórica) de combustión del combustible.
Las pérdidas de calor a través de las paredes de los hornos hacia el exterior (hacia el medio ambiente) reducen la temperatura de combustión del combustible.
Combustión de combustible
La combustión de combustible es un proceso de oxidación de componentes combustibles que se produce a altas temperaturas y va acompañado de la liberación de calor. La naturaleza de la combustión está determinada por muchos factores, incluido el método de combustión, el diseño del horno, la concentración de oxígeno, etc. Pero las condiciones del curso, la duración y los resultados finales de los procesos de combustión dependen en gran medida de la composición. , características físicas y químicas del combustible.
Composición del combustible
Los combustibles sólidos incluyen carbón y lignito, turba, pizarra bituminosa y madera. Estos tipos de combustibles son compuestos orgánicos complejos formados principalmente por cinco elementos: carbono C, hidrógeno H, oxígeno O, azufre S y nitrógeno N. La composición del combustible también incluye humedad y minerales no combustibles, que forman cenizas después de la combustión. La humedad y las cenizas son lastre de combustible externo, mientras que el oxígeno y el nitrógeno son internos.
El elemento principal de la parte combustible es el carbono, determina la liberación de la mayor cantidad de calor. Sin embargo, cuanto mayor es la proporción de carbono en un combustible sólido, más difícil es encenderlo. Durante la combustión, el hidrógeno libera 4,4 veces más calor que el carbono, pero su participación en la composición de los combustibles sólidos es pequeña. El oxígeno, al no ser un elemento generador de calor y unir hidrógeno y carbono, reduce el calor de combustión, por lo que es un elemento indeseable. Su contenido es especialmente elevado en turba y madera. La cantidad de nitrógeno en los combustibles sólidos es pequeña, pero es capaz de formar óxidos dañinos para el medio ambiente y los seres humanos. El azufre también es una impureza nociva, emite poco calor, pero los óxidos resultantes provocan la corrosión del metal de las calderas y la contaminación de la atmósfera.
Especificaciones del combustible y su influencia en el proceso de combustión
Las características técnicas más importantes del combustible son: calor de combustión, rendimiento de sustancias volátiles, propiedades de residuo no volátil (coque), contenido de cenizas y contenido de humedad.
Calor de combustión del combustible
El poder calorífico es la cantidad de calor liberado durante la combustión completa de una unidad de masa (kJ / kg) o volumen de combustible (kJ / m3). Distinga entre calor de combustión más alto y más bajo. El más alto incluye el calor liberado durante la condensación de los vapores contenidos en los productos de combustión. Cuando se quema combustible en hornos de caldera, los gases de combustión de escape tienen una temperatura a la que la humedad se encuentra en estado de vapor. Por tanto, en este caso, se utiliza un menor calor de combustión, que no tiene en cuenta el calor de condensación del vapor de agua.
La composición y el poder calorífico neto de todos los depósitos de carbón conocidos se han determinado y dado en las características calculadas.
Liberación de materia volátil
Cuando el combustible sólido se calienta sin acceso al aire bajo la influencia de altas temperaturas, primero se libera vapor de agua y luego se produce la descomposición térmica de las moléculas con la liberación de sustancias gaseosas, llamadas sustancias volátiles.
La liberación de sustancias volátiles puede ocurrir en el rango de temperatura de 160 a 1100 ° C, pero en promedio, en el rango de temperatura de 400-800 ° C. La temperatura de inicio de la liberación de volátiles, la cantidad y composición de productos gaseosos dependen de la composición química del combustible. Cuanto más antiguo químicamente es el combustible, menor es la liberación de volátiles y mayor es la temperatura de inicio de su liberación.
Los volátiles proporcionan una ignición más temprana del material particulado y tienen un efecto significativo en la combustión del combustible. Los combustibles jóvenes (turba, lignito) se encienden fácilmente, se queman rápidamente y casi por completo. Por el contrario, los combustibles con bajos volátiles, como la antracita, son más difíciles de encender, se queman mucho más lentamente y no se queman por completo (con una mayor pérdida de calor).
Propiedades de los residuos no volátiles (coque)
La parte sólida del combustible que queda después de la liberación de volátiles, que consiste principalmente en carbono y una parte mineral, se llama coque. El residuo de coque puede ser, dependiendo de las propiedades de los compuestos orgánicos incluidos en la masa combustible: apelmazado, ligeramente apelmazado (degradado por exposición), pulverulento. La antracita, la turba y el lignito dan un residuo pulverulento no volátil. La mayoría de los carbones bituminosos están sinterizados, pero no siempre con fuerza. Los residuos no volátiles pegajosos o pulverulentos dan carbones bituminosos con un rendimiento muy alto de volátiles (42-45%) y con un rendimiento muy bajo (menos del 17%).
La estructura del residuo de coque es importante cuando se quema carbón en hornos de parrilla.Cuando se quema en calderas eléctricas, el rendimiento del coque no es muy importante.
Contenido de cenizas
El combustible sólido contiene la mayor cantidad de impurezas minerales no combustibles. Estos son principalmente arcilla, silicatos, pirita, pero también se pueden incluir óxido ferroso, sulfatos, carbonatos y silicatos de hierro, óxidos de varios metales, cloruros, álcalis, etc. La mayoría de ellos caen durante la extracción en forma de rocas, entre las que se encuentran las vetas de carbón, pero también hay sustancias minerales que han pasado al combustible desde los formadores de carbón o en el proceso de convertir su masa original.
Cuando se quema combustible, las impurezas minerales sufren una serie de reacciones, como resultado de lo cual se forma un residuo sólido no combustible llamado ceniza. El peso y la composición de la ceniza no son idénticos al peso y la composición de las impurezas minerales del combustible.
Las propiedades de las cenizas juegan un papel importante en la organización del funcionamiento de la caldera y el horno. Sus partículas, arrastradas por los productos de combustión, a altas velocidades desgastan las superficies de calentamiento, y a bajas velocidades se depositan sobre ellas, lo que conduce a un deterioro de la transferencia de calor. Las cenizas arrastradas a la chimenea pueden dañar el medio ambiente, para evitar esto, se requiere la instalación de recolectores de cenizas.
Una propiedad importante de las cenizas es su fusibilidad; distinguen entre cenizas refractarias (por encima de 1425 ° C), de fusión media (1200-1425 ° C) y de fusión baja (menos de 1200 ° C). La ceniza que ha pasado la etapa de fusión y se convierte en una masa sinterizada o fusionada se llama escoria. La característica de temperatura de la fusibilidad de las cenizas es de gran importancia para asegurar el funcionamiento confiable de las superficies del horno y la caldera; la elección correcta de la temperatura de los gases cerca de estas superficies eliminará la escoria.
Contenido de humedad
La humedad es un componente indeseable del combustible, junto con las impurezas minerales, es lastre y reduce el contenido de la parte combustible. Además, reduce el valor térmico, ya que se requiere energía adicional para su evaporación.
La humedad del combustible puede ser interna o externa. La humedad externa está contenida en los capilares o atrapada en la superficie. Con la edad química, la cantidad de humedad capilar disminuye. Cuanto más pequeñas son las piezas de combustible, mayor es la humedad de la superficie. La humedad interna ingresa a la materia orgánica.
El contenido de humedad en el combustible reduce el calor de combustión y conduce a un aumento en el consumo de combustible. Al mismo tiempo, aumentan los volúmenes de productos de combustión, aumentan las pérdidas de calor con los gases de escape y disminuye la eficiencia de la unidad de caldera. La alta humedad en invierno conduce a la congelación del carbón, dificultades para moler y una disminución de la fluidez.
Métodos de combustión de combustible según el tipo de horno.
Los principales tipos de dispositivos de combustión:
- en capas
- cámara.
Hornos de capas están destinados a la combustión de combustible sólido en grumos. Pueden ser densos y fluidizados. Cuando se quema en una capa densa, el aire de combustión pasa a través de la capa sin afectar su estabilidad, es decir, la gravedad de las partículas en combustión excede la presión dinámica del aire. Cuando se quema en un lecho fluidizado, debido al aumento de la velocidad del aire, las partículas entran en un estado de "ebullición". En este caso, se produce una mezcla activa del oxidante y el combustible, por lo que se intensifica la combustión del combustible.
A hornos de cámara quemar combustible sólido pulverizado, así como líquido y gaseoso. Los hornos de cámara se subdividen en ciclónicos y antorcha. Durante la combustión de la llamarada, las partículas de carbón no deben tener más de 100 micrones, se queman en el volumen de la cámara de combustión. La combustión ciclónica permite un tamaño de partícula más grande; bajo la influencia de las fuerzas centrífugas, se arrojan a las paredes del horno y se queman por completo en un flujo arremolinado en una zona de alta temperatura.
Combustión de combustible. Las principales etapas del proceso
En el proceso de quema de combustibles sólidos se pueden distinguir ciertas etapas: calentamiento y evaporación de la humedad, sublimación de volátiles y formación de residuos de coque, combustión de volátiles y coque, y formación de escoria. Esta división del proceso de combustión es relativamente arbitraria, ya que aunque estas etapas proceden secuencialmente, se superponen parcialmente entre sí. Entonces, la sublimación de las sustancias volátiles comienza antes de la evaporación final de toda la humedad, la formación de los volátiles ocurre simultáneamente con el proceso de su combustión, así como el inicio de la oxidación del residuo de coque precede al final de la combustión de los volátiles, y el la postcombustión del coque también puede tener lugar después de la formación de escoria.
El tiempo de flujo de cada etapa del proceso de combustión está determinado en gran medida por las propiedades del combustible. La etapa de combustión del coque es la que más dura, incluso para combustibles con alto rendimiento volátil. Varios factores operativos y características de diseño del horno tienen un impacto significativo en la duración de las etapas del proceso de combustión.
1. Preparación del combustible antes del encendido.
El combustible que ingresa al horno se calienta, como resultado de lo cual, en presencia de humedad, se evapora y el combustible se seca. El tiempo necesario para calentar y secar depende de la cantidad de humedad y la temperatura a la que se suministra el combustible al dispositivo de combustión. Para combustibles con un alto contenido de humedad (turba, carbones pardos húmedos), la etapa de calentamiento y secado es relativamente larga.
El combustible se suministra a los hornos apilados a una temperatura cercana a la temperatura ambiente. Solo en invierno, cuando el carbón se congela, su temperatura es más baja que en la sala de calderas. Para la combustión en hornos de antorcha y vórtice, el combustible se somete a trituración y trituración, acompañado de secado con aire caliente o gases de combustión. Cuanto mayor sea la temperatura del combustible entrante, se necesitará menos tiempo y calor para calentarlo hasta la temperatura de ignición.
El secado del combustible en el horno se produce debido a dos fuentes de calor: calor convectivo de los productos de combustión y calor radiante de un soplete, revestimiento y escoria.
En los hornos de cámara, el calentamiento se realiza principalmente a expensas de la primera fuente, es decir, mezclando los productos de combustión con el combustible en el punto de su entrada. Por lo tanto, uno de los requisitos importantes para el diseño de dispositivos para introducir combustible en el horno es garantizar una succión intensiva de los productos de combustión. Una temperatura más alta en la cámara de combustión también contribuye a un tiempo de calentamiento y secado más corto. Para ello, cuando se queman combustibles con el inicio de la liberación de volátiles a altas temperaturas (más de 400 ° C), se fabrican bandas incendiarias en hornos de cámara, es decir, cierran las tuberías de blindaje con un material refractario termoaislante en para reducir su percepción del calor.
Al quemar combustible en un lecho, la función de cada tipo de fuente de calor está determinada por el diseño del horno. En los hornos con rejillas de cadena, el calentamiento y el secado se realizan principalmente mediante el calor radiante de la antorcha. En los hornos con parrilla fija y suministro de combustible desde arriba, el calentamiento y secado se produce debido a que los productos de combustión se mueven a través de la capa de abajo hacia arriba.
En el proceso de calentamiento a una temperatura superior a 110 ° C, comienza la descomposición térmica de las sustancias orgánicas que componen los combustibles. Los compuestos menos fuertes son aquellos que contienen una cantidad significativa de oxígeno. Estos compuestos se descomponen a temperaturas relativamente bajas con la formación de volátiles y un residuo sólido, que consiste principalmente en carbono.
Los combustibles que son jóvenes en composición química, que contienen mucho oxígeno, tienen una baja temperatura de inicio de la liberación de sustancias gaseosas y dan un mayor porcentaje de ellas. Los combustibles con un bajo contenido de compuestos de oxígeno tienen un rendimiento de baja volatilidad y un punto de inflamación más alto.
El contenido de moléculas en combustibles sólidos que se descomponen fácilmente cuando se calientan también afecta la reactividad del residuo no volátil.Primero, la descomposición de la masa combustible ocurre principalmente en la superficie exterior del combustible. Con un mayor calentamiento, las reacciones pirogenéticas comienzan a ocurrir dentro de las partículas de combustible, la presión aumenta en ellas y la capa exterior se rompe. Cuando se queman combustibles con un alto rendimiento de volátiles, el residuo de coque se vuelve poroso y tiene una superficie más grande en comparación con el residuo sólido denso.
2. El proceso de combustión de compuestos gaseosos y coque
La combustión real de combustible comienza con la ignición de sustancias volátiles. Durante el período de preparación del combustible, ocurren reacciones en cadena ramificada de oxidación de sustancias gaseosas, al principio estas reacciones proceden a velocidades bajas. El calor liberado es percibido por las superficies del horno y se acumula parcialmente en forma de energía de moléculas en movimiento. Esto último conduce a un aumento en la velocidad de las reacciones en cadena. A cierta temperatura, las reacciones de oxidación se desarrollan a tal velocidad que el calor liberado cubre completamente la absorción de calor. Esta temperatura es el punto de inflamación.
La temperatura de ignición no es constante, depende tanto de las propiedades del combustible como de las condiciones en la zona de ignición, en promedio es de 400-600 ° C. Después de la ignición de la mezcla gaseosa, una mayor autoaceleración de las reacciones de oxidación provoca un aumento de temperatura. Para mantener la combustión, se requiere un suministro continuo de oxidantes y sustancias combustibles.
La ignición de sustancias gaseosas conduce a la envoltura de la partícula de coque en una envoltura de fuego. La combustión del coque comienza cuando finaliza la combustión de volátiles. La partícula sólida se calienta a una temperatura alta y, a medida que disminuye la cantidad de volátiles, el grosor de la capa límite de combustión disminuye, el oxígeno llega a la superficie del carbón caliente.
La combustión del coque comienza a una temperatura de 1000 ° C y es el proceso más largo. La razón es que, en primer lugar, la concentración de oxígeno disminuye y, en segundo lugar, las reacciones heterogéneas proceden más lentamente que las homogéneas. Como resultado, la duración de la combustión de una partícula de combustible sólido está determinada principalmente por el tiempo de combustión del residuo de coque (aproximadamente 2/3 del tiempo total). Para combustibles con alto rendimiento de volátiles, el residuo sólido es menos de la mitad de la masa de partículas inicial, por lo tanto, su combustión ocurre rápidamente y la posibilidad de subcombustión es baja. Los combustibles químicamente viejos tienen una partícula densa, cuya combustión lleva casi todo el tiempo que se pasa en el horno.
El residuo de coque de la mayoría de los combustibles sólidos está compuesto principalmente por carbono, y para algunas especies. La combustión de carbono sólido ocurre con la formación de monóxido de carbono y dióxido de carbono.
Condiciones óptimas para la disipación del calor.
La creación de condiciones óptimas para la combustión de carbono es la base para la correcta construcción de un método tecnológico para quemar combustibles sólidos en unidades de caldera. Los siguientes factores pueden influir en el logro de la mayor liberación de calor en el horno: temperatura, exceso de aire, formación de mezcla primaria y secundaria.
La temperatura... La liberación de calor durante la combustión del combustible depende significativamente del régimen de temperatura del horno. A temperaturas relativamente bajas, se produce una combustión incompleta de sustancias combustibles en el núcleo de la antorcha; el monóxido de carbono, el hidrógeno y los hidrocarburos permanecen en los productos de combustión. A temperaturas de 1000 a 1800-2000 ° C, se puede lograr la combustión completa del combustible.
Exceso de aire... La generación de calor específico alcanza su valor máximo con una combustión completa y una relación de aire en exceso de la unidad. Con una disminución en la relación de exceso de aire, la liberación de calor disminuye, ya que la falta de oxígeno conduce a la oxidación de menos combustible. El nivel de temperatura disminuye, las velocidades de reacción disminuyen, lo que conduce a una fuerte disminución en la liberación de calor.
Un aumento en la relación de exceso de aire superior a uno reduce la generación de calor incluso más que la falta de aire.En condiciones reales de combustión de combustible en hornos de caldera, no se alcanzan los valores límite de liberación de calor, ya que existe una combustión incompleta. Depende en gran medida de cómo estén organizados los procesos de formación de la mezcla.
Procesos de mezcla... En los hornos de cámara, la mezcla primaria se logra secando y mezclando el combustible con aire, suministrando parte del aire (primario) a la zona de preparación, creando un soplete bien abierto con una amplia superficie y alta turbulización, utilizando aire caliente.
En los hornos de capas, la tarea de mezcla principal es suministrar la cantidad requerida de aire a las diferentes zonas de combustión en la parrilla.
Para asegurar la postcombustión de productos gaseosos de combustión incompleta y coque, se organizan procesos de formación de mezclas secundarias. Estos procesos se ven facilitados por: el suministro de aire secundario a alta velocidad, la creación de dicha aerodinámica, en la que se logra el llenado uniforme de todo el horno con un soplete y, en consecuencia, el tiempo de residencia de los gases y partículas de coque en el horno. aumenta.
3. Formación de escoria
En el proceso de oxidación de la masa combustible de combustible sólido, también ocurren cambios significativos en las impurezas minerales. Las sustancias de bajo punto de fusión y las aleaciones con un bajo punto de fusión disuelven los compuestos refractarios.
Un requisito previo para el funcionamiento normal de las calderas es la eliminación ininterrumpida de los productos de combustión y la escoria resultante.
Durante la combustión de la capa, la formación de escoria puede provocar una combustión inferior mecánica: las impurezas minerales envuelven las partículas de coque no quemadas, o la escoria viscosa puede bloquear los conductos de aire, bloqueando el acceso de oxígeno al coque en combustión. Para reducir la subcombustión, se utilizan varias medidas: en hornos con rejillas de cadena, se aumenta el tiempo que se pasa en la rejilla de escoria y se realiza un corte frecuente.
En hornos estratificados, la escoria se elimina en forma seca. En los hornos de cámara, la eliminación de la escoria puede ser seca o líquida.
Así, la combustión de combustibles es un proceso fisicoquímico complejo, en el que influyen una gran cantidad de factores diferentes, pero todos ellos deben tenerse en cuenta a la hora de diseñar calderas y hornos.
Combustión - gasolina
La combustión de gasolina con detonación se acompaña de la aparición de golpes metálicos agudos, humo negro en el escape, un aumento en el consumo de gasolina, una disminución en la potencia del motor y otros fenómenos negativos.
La combustión de gasolina en el motor también depende de la relación de exceso de aire. En los valores a 0 9 - j - 1 1, la tasa de procesos de oxidación previa a la llama en la mezcla de trabajo es la más alta. Por lo tanto, a estos valores de a, se crean las condiciones más favorables para el inicio de la detonación.
Después de la combustión de la gasolina, la masa total de dichos contaminantes aumentó significativamente junto con la redistribución general de sus cantidades. El porcentaje de benceno en el condensado de los gases de escape de los automóviles era aproximadamente de 1 a 7 veces mayor que el de la gasolina; el contenido de tolueno fue 3 veces mayor y el contenido de xileno fue 30 veces mayor. Se sabe que en este caso se forman compuestos de oxígeno, y el número de iones, característico de los compuestos insaturados más pesados de las series de olefinas o cicloparafinas y acetileno o dieno, especialmente esta última, aumenta bruscamente. En términos generales, los cambios en la cámara de Haagen-Smit se asemejaron a los cambios necesarios para hacer que la composición de las muestras de escape de vehículos típicas sea similar a las de la muestra de smog de Los Ángeles.
El poder calorífico de la gasolina depende de su composición química. Por tanto, los hidrocarburos ricos en hidrógeno (por ejemplo, los parafínicos) tienen una gran masa de calor de combustión.
Los productos de combustión de gasolina se expanden en el motor de combustión interna a lo largo del politropo n1 27 de 30 a 3 en. La temperatura inicial de los gases es 2100 C; la composición másica de los productos de combustión de 1 kg de gasolina es la siguiente: CO23 135 kg, H2 1305 kg, O20 34 kg, N2 12 61 kg.Determine el trabajo de expansión de estos gases, si se introducen 2 g de gasolina en el cilindro al mismo tiempo.
| Influencia de TPP en la formación de carbono en el motor. |
Cuando se quema gasolina de una planta de energía térmica, se forman depósitos de carbón que contienen óxido de plomo.
Cuando se quema gasolina en motores alternativos de combustión interna, casi todos los productos formados se llevan con los gases de escape. Solo una parte relativamente pequeña de los productos de la combustión incompleta de combustible y aceite, una pequeña cantidad de compuestos inorgánicos formados a partir de elementos introducidos con combustible, aire y aceite, se deposita en forma de depósitos de carbono.
Cuando la gasolina se quema con tetraetilo de plomo, aparentemente se forma óxido de plomo, que se derrite solo a una temperatura de 900 C y puede evaporarse a una temperatura muy alta, superando la temperatura promedio en el cilindro del motor. Para evitar la deposición de óxido de plomo en el motor, se introducen sustancias especiales en el líquido de etilo: captadores. Los hidrocarburos halogenados se utilizan como depuradores. Por lo general, estos son compuestos que contienen bromo y cloro, que también queman y unen el plomo en nuevos compuestos de bromuro y cloruro.
| Influencia de TPP en la formación de carbono en el motor. |
Cuando se quema gasolina de una planta de energía térmica, se forman depósitos de carbón que contienen óxido de plomo.
Durante la combustión de gasolina que contiene TPP puro, se deposita una placa de compuestos de plomo en el motor. La composición del grado líquido de etilo R-9 (en peso): tetraetil plomo 54 0%, bromoetano 33 0%, monocloronaftaleno 6 8 0 5%, relleno - aviación - gasolina - hasta 100%; tinte rojo oscuro 1 g por 1 kg de la mezcla.
Cuando se quema gasolina que contiene TPP, se forma óxido de fístula con baja volatilidad en el motor; Dado que el punto de fusión del óxido de plomo es bastante alto (888), parte de él (alrededor del 10%, contando con el plomo introducido con la gasolina) se deposita como un residuo sólido en las paredes de la cámara de combustión, velas y válvulas, lo que conduce a una falla rápida del motor.
Cuando se quema gasolina en el motor de un automóvil, también se forman moléculas más pequeñas y la energía liberada se distribuye en un volumen mayor.
Los gases incandescentes de la combustión de gasolina fluyen alrededor del intercambiador de calor 8 (en el interior desde el lado de la cámara de combustión y más allá, a través de las ventanas 5 en el exterior, pasando por la cámara de gases de escape 6) y calientan el aire en el canal del intercambiador de calor. A continuación, los gases de escape calientes se alimentan a través del tubo de escape 7 debajo del cárter y calientan el motor desde el exterior, y el aire caliente del intercambiador de calor se alimenta a través del respiradero al cárter y calienta el motor desde el interior. En 1 5 a 2 minutos después del inicio del calentamiento, la bujía incandescente se apaga y la combustión en el calentador continúa sin su participación. Después de 7 a 13 minutos desde el momento de recibir un pulso para arrancar el motor, el aceite en el cárter se calienta a una temperatura de 30 C (a una temperatura ambiente de hasta -25 C) y los pulsos de arranque de la unidad son suministrado, después de lo cual se apaga el calentador.
Temperatura de combustión
En ingeniería térmica, se distinguen las siguientes temperaturas de combustión de los gases: producción de calor, calorimétrica, teórica y real (calculada). La capacidad calorífica tx es la temperatura máxima de los productos de la combustión completa del gas en condiciones adiabáticas con un coeficiente de exceso de aire a = 1,0 y una temperatura del gas y del aire igual a 0 ° C:
tx = Qh / (IVcv) (8.11)
donde QH es el valor calorífico más bajo del gas, kJ / m3; IVcp - la suma de los productos de los volúmenes de dióxido de carbono, vapor de agua y nitrógeno formados durante la combustión de 1 m3 de gas (m3 / m3) y sus capacidades caloríficas volumétricas promedio a presión constante dentro del rango de temperatura de 0 ° С a tx (kJ / (m3 * ° С).
Debido a la inconstancia de la capacidad calorífica de los gases, la producción de calor se determina mediante el método de aproximaciones sucesivas. Como parámetro inicial se toma su valor para gas natural (= 2000 ° C), con a = 1.0, se determinan los volúmenes de los componentes de los productos de combustión, según tabla.8.3, se calcula su capacidad calorífica media y luego, de acuerdo con la fórmula (8.11), se calcula la capacidad calorífica del gas. Si, como resultado del cálculo, resulta ser más bajo o más alto que el aceptado, entonces se establece una temperatura diferente y se repite el cálculo. La producción de calor de los gases comunes simples y complejos cuando se queman en aire seco se da en la tabla. 8.5. Cuando se quema gas en aire atmosférico que contiene aproximadamente 1 wt. % de humedad, la producción de calor disminuye en 25-30 ° С.
La temperatura de combustión calorimétrica tK es la temperatura determinada sin tener en cuenta la disociación del vapor de agua y el dióxido de carbono, pero teniendo en cuenta la temperatura inicial real del gas y el aire. Se diferencia de la producción de calor tx en que las temperaturas del gas y del aire, así como el coeficiente de aire en exceso a, se toman de sus valores reales. Puede determinar tK mediante la fórmula:
tк = (Qн + qphys) / (ΣVcp) (8.12)
donde qphys es el contenido de calor (calor físico) del gas y el aire, medido desde 0 ° C, kJ / m3.
Los gases de petróleo naturales y licuados generalmente no se calientan antes de la combustión y su volumen en comparación con el volumen de aire de combustión es pequeño.
Cuadro 8.3.
Capacidad calorífica volumétrica media de los gases, kJ / (m3 • ° С)
| Ttemperatura, ° С | CO2 | N2 | O2 | CO | CH4 | H2 | H2O (vapor de agua) | aire | |
| seco | húmedo por m3 de gas seco pero | ||||||||
| 0 | 1,5981 | 1,2970 | 1,3087 | 1,3062 | 1,5708 | 1,2852 | 1,4990 | 1,2991 | 1,3230 |
| 100 | 1,7186 | 1,2991 | 1,3209 | 1,3062 | 1,6590 | 1,2978 | 1,5103 | 1,3045 | 1,3285 |
| 200 | 1,8018 | 1,3045 | 1,3398 | 1,3146 | 1,7724 | 1,3020 | 1,5267 | 1,3142 | 1,3360 |
| 300 | 1,8770 | 1,3112 | 1,3608 | 1,3230 | 1,8984 | 1,3062 | 1,5473 | 1,3217 | 1,3465 |
| 400 | 1,9858 | 1,3213 | 1,3822 | 1,3356 | 2,0286 | 1,3104 | 1,5704 | 1,3335 | 1,3587 |
| 500 | 2,0030 | 1,3327 | 1,4024 | 1,3482 | 2,1504 | 1,3104 | 1,5943 | 1,3469 | 1,3787 |
| 600 | 2,0559 | 1,3453 | 1,4217 | 1,3650 | 2,2764 | 1,3146 | 1,6195 | 1,3612 | 1,3873 |
| 700 | 2,1034 | 1,3587 | 1,3549 | 1,3776 | 2,3898 | 1,3188 | 1,6464 | 1,3755 | 1,4020 |
| 800 | 2,1462 | 1,3717 | 1,4549 | 1,3944 | 2,5032 | 1,3230 | 1,6737 | 1,3889 | 1,4158 |
| 900 | 2,1857 | 1,3857 | 1,4692 | 1,4070 | 2,6040 | 1,3314 | 1,7010 | 1,4020 | 1,4293 |
| 1000 | 2,2210 | 1,3965 | 1,4822 | 1,4196 | 2,7048 | 1,3356 | 1,7283 | 1,4141 | 1,4419 |
| 1100 | 2,2525 | 1,4087 | 1,4902 | 1,4322 | 2,7930 | 1,3398 | 1,7556 | 1,4263 | 1,4545 |
| 1200 | 2,2819 | 1,4196 | 1,5063 | 1,4448 | 2,8812 | 1,3482 | 1,7825 | 1,4372 | 1,4658 |
| 1300 | 2,3079 | 1,4305 | 1,5154 | 1,4532 | — | 1,3566 | 1,8085 | 1,4482 | 1,4771 |
| 1400 | 2,3323 | 1,4406 | 1,5250 | 1,4658 | — | 1,3650 | 1,8341 | 1,4582 | 1,4876 |
| 1500 | 2,3545 | 1,4503 | 1,5343 | 1,4742 | — | 1,3818 | 1,8585 | 1,4675 | 1,4973 |
| 1600 | 2,3751 | 1,4587 | 1,5427 | — | — | — | 1,8824 | 1,4763 | 1,5065 |
| 1700 | 2,3944 | 1,4671 | 1,5511 | — | — | — | 1,9055 | 1,4843 | 1,5149 |
| 1800 | 2,4125 | 1,4746 | 1,5590 | — | — | — | 1,9278 | 1,4918 | 1,5225 |
| 1900 | 2,4289 | 1,4822 | 1,5666 | — | — | — | 1,9698 | 1,4994 | 1,5305 |
| 2000 | 2,4494 | 1,4889 | 1,5737 | 1,5078 | — | — | 1,9694 | 1,5376 | 1,5376 |
| 2100 | 2,4591 | 1,4952 | 1,5809 | — | — | — | 1,9891 | — | — |
| 2200 | 2,4725 | 1,5011 | 1,5943 | — | — | — | 2,0252 | — | — |
| 2300 | 2,4860 | 1,5070 | 1,5943 | — | — | — | 2,0252 | — | — |
| 2400 | 2,4977 | 1,5166 | 1,6002 | — | — | — | 2,0389 | — | — |
| 2500 | 2,5091 | 1,5175 | 1,6045 | — | — | — | 2,0593 | — | — |
Por lo tanto, al determinar la temperatura calorimétrica, se puede ignorar el contenido de calor de los gases. Cuando se queman gases de bajo poder calorífico (generador, alto horno, etc.), su contenido de calor (especialmente calentado antes de la combustión) tiene un efecto muy significativo sobre la temperatura calorimétrica.
La dependencia de la temperatura calorimétrica del gas natural de composición media en el aire con una temperatura de 0 ° C y una humedad del 1% del coeficiente de aire en exceso a se da en la Tabla. 8.5, para GLP cuando se quema en aire seco - en tabla. 8.7. Datos de la tabla. 8.5-8.7 es posible guiarse con suficiente precisión al establecer la temperatura calorimétrica de combustión de otros gases naturales, que son relativamente similares en composición, y gases de hidrocarburos de casi cualquier composición. Si es necesario obtener una temperatura alta al quemar gases con bajos coeficientes de aire en exceso, así como aumentar la eficiencia de los hornos, en la práctica, el aire se calienta, lo que conduce a un aumento de la temperatura calorimétrica (ver Tabla 8.6). .
Cuadro 8.4.
Capacidad calorífica de gases en aire seco
| Gas simple | Capacidad de calefacción, ° С | Gas complejo de composición media | Salida de calor aproximada, ° С |
| Hidrógeno | 2235 | Campos de gas natural | 2040 |
| Monóxido de carbono | 2370 | Campos de petróleo natural | 2080 |
| Metano | 2043 | Coca | 2120 |
| Etano | 2097 | Destilación de esquisto a alta temperatura | 1980 |
| Propano | 2110 | Explosión de vapor-oxígeno a presión | 2050 |
| Butano | 2118 | Generador de carbón graso | 1750 |
| Pentano | 2119 | Generador de chorro de vapor y aire a partir de combustibles pobres | 1670 |
| Etileno | 2284 | Licuado (50% C3H4 + 50% C4H10) | 2115 |
| Acetileno | 2620 | Agua | 2210 |
Cuadro 8.5.
Temperaturas calorimétricas y teóricas de combustión de gas natural en aire con t = 0 ° С y humedad 1% * dependiendo del coeficiente de aire en exceso a
| Relación de exceso de aire a | Calorimétrico temperatura de combustión tк, ° С | Teórico temperatura de combustión | Relación de exceso de aire a | Calorimétrico temperatura de combustión tк, ° С |
| 1,0 | 2010 | 1920 | 1,33 | 1620 |
| 1,02 | 1990 | 1900 | 1,36 | 1600 |
| 1,03 | 1970 | 1880 | 1,40 | 1570 |
| 1,05 | 1940 | 1870 | 1,43 | 1540 |
| 1,06 | 1920 | 1860 | 1,46 | 1510 |
| 1,08 | 1900 | 1850 | 1,50 | 1470 |
| 1,10 | 1880 | 1840 | 1,53 | 1440 |
| 1,12 | 1850 | 1820 | 1,57 | 1410 |
| 1,14 | 1820 | 1790 | 1,61 | 1380 |
| 1,16 | 1800 | 1770 | 1,66 | 1350 |
| 1,18 | 1780 | 1760 | 1,71 | 1320 |
| 1,20 | 1760 | 1750 | 1,76 | 1290 |
| 1,22 | 1730 | — | 1,82 | 1260 |
| 1,25 | 1700 | — | 1,87 | 1230 |
| 1,28 | 1670 | — | 1,94 | 1200 |
| 1,30 | 1650 | — | 2,00 | 1170 |
>
La temperatura de combustión teórica tT es la temperatura máxima determinada de manera similar a la temperatura calorimétrica tK, pero con una corrección por reacciones endotérmicas (que requieren calor) de disociación de dióxido de carbono y vapor de agua, procediendo con un aumento de volumen:
СО2 ‹–› СО + 0.5О2 - 283 mJ / mol (8.13)
Н2О ‹–› Н2 + 0.5О2 - 242 mJ / mol (8.14)
A altas temperaturas, la disociación puede conducir a la formación de hidrógeno atómico, oxígeno y grupos hidroxilo OH. Además, cuando se quema el gas, siempre se genera algo de óxido de nitrógeno. Todas estas reacciones son endotérmicas y conducen a una disminución de la temperatura de combustión.
Cuadro 8.6.
Temperatura calorimétrica de combustión de gas natural tу, ° С, dependiendo de la relación de exceso de aire seco y su temperatura (valores redondeados)
| Relación de exceso de aire a | Temperatura del aire seco, ° С | ||||||||
| 20 | 100 | 200 | 300 | 400 | 500 | 600 | 700 | 800 | |
| 0,5 | 1380 | 1430 | 1500 | 1545 | 1680 | 1680 | 1740 | 1810 | 1860 |
| 0,6 | 1610 | 1650 | 1715 | 1780 | 1840 | 1900 | 1960 | 2015 | 2150 |
| 0,7 | 1730 | 1780 | 1840 | 1915 | 1970 | 2040 | 2100 | 2200 | 2250 |
| 0,8 | 1880 | 1940 | 2010 | 2060 | 2130 | 2200 | 2260 | 2330 | 2390 |
| 0,9 | 1980 | 2030 | 2090 | 2150 | 2220 | 2290 | 2360 | 2420 | 2500 |
| 1,0 | 2050 | 2120 | 2200 | 2250 | 2320 | 2385 | 2450 | 2510 | 2560 |
| 1,2 | 1810 | 1860 | 1930 | 2000 | 2070 | 2140 | 2200 | 2280 | 2350 |
| 1,4 | 1610 | 1660 | 1740 | 1800 | 2870 | 1950 | 2030 | 2100 | 2160 |
| 1,6 | 1450 | 1510 | 1560 | 1640 | 1730 | 1800 | 1860 | 1950 | 2030 |
| 1,8 | 1320 | 1370 | 1460 | 1520 | 1590 | 1670 | 1740 | 1830 | 1920 |
| 2,0 | 1220 | 1270 | 1360 | 1420 | 1490 | 1570 | 1640 | 1720 | 1820 |
Cuadro 8.7.
Temperatura de combustión calorimétrica tK del propano comercial en aire seco con t = 0 ° С dependiendo del coeficiente de aire en exceso a
| Relación de exceso de aire a | Temperatura de combustión calorimétrica tH, ° С | Relación de exceso de aire a | Temperatura de combustión calorimétrica tK, ° С |
| 1,0 | 2110 | 1,45 | 1580 |
| 1,02 | 2080 | 1,48 | 1560 |
| 1,04 | 2050 | 1,50 | 1540 |
| 1,05 | 2030 | 1,55 | 1500 |
| 1,07 | 2010 | 1,60 | 1470 |
| 1,10 | 1970 | 1,65 | 1430 |
| 1,12 | 1950 | 1,70 | 1390 |
| 1,15 | 1910 | 1,75 | 1360 |
| 1,20 | 1840 | 1,80 | 1340 |
| 1,25 | 1780 | 1,85 | 1300 |
| 1,27 | 1750 | 1,90 | 1270 |
| 1,30 | 1730 | 1,95 | 1240 |
| 1,35 | 1670 | 2,00 | 1210 |
| 1,40 | 1630 | 2,10 | 1170 |
La temperatura de combustión teórica se puede determinar mediante la siguiente fórmula:
tT = (Qн + qphys - qdis) / (ΣVcp) (8.15)
donde qduc es el consumo total de calor para la disociación de СО2 y Н2О en productos de combustión, kJ / m3; IVcp: la suma del producto del volumen y la capacidad calorífica promedio de los productos de combustión, teniendo en cuenta la disociación por 1 m3 de gas.
Como puede ver en la tabla. 8.8, a temperaturas de hasta 1600 ° C, el grado de disociación puede ignorarse y la temperatura de combustión teórica puede tomarse igual a la temperatura calorimétrica. A temperaturas más altas, el grado de disociación puede reducir significativamente la temperatura en el espacio de trabajo. En la práctica, no existe una necesidad particular para esto, la temperatura de combustión teórica debe determinarse solo para hornos de alta temperatura que funcionan con aire precalentado (por ejemplo, hornos de hogar abierto). No es necesario para las plantas de calderas.
La temperatura real (calculada) de los productos de combustión td es la temperatura que se alcanza en condiciones reales en el punto más caliente de la llama. Es menor que el teórico y depende de la pérdida de calor al ambiente, el grado de transferencia de calor de la zona de combustión por radiación, la duración del proceso de combustión en el tiempo, etc. de la temperatura en los hornos con la introducción de factores de corrección establecidos experimentalmente en ellos:
td = t (8.16)
donde n - t. n. coeficiente pirométrico dentro de:
- para hornos térmicos y de calefacción de alta calidad con aislamiento térmico: 0,75-0,85;
- para hornos sellados sin aislamiento térmico - 0,70-0,75;
- para hornos de caldera blindados - 0,60-0,75.
En la práctica, es necesario conocer no solo las temperaturas de combustión adiabática dadas anteriormente, sino también las temperaturas máximas que ocurren en la llama. Sus valores aproximados suelen establecerse experimentalmente mediante métodos espectrográficos. Las temperaturas máximas que surgen en una llama libre a una distancia de 5-10 mm desde la parte superior del frente de combustión cónico se dan en la tabla. 8,9. Un análisis de los datos presentados muestra que las temperaturas máximas en la llama son menores que la salida de calor (debido al consumo de calor para la disociación de H2O y CO2 y la remoción de calor de la zona de la llama).
- hogar
- Directorio
- Características de combustión de los gases.
- Temperatura de combustión
Combustión - producto de aceite
La combustión de productos petrolíferos en el terraplén del parque de tanques se elimina mediante el suministro inmediato de espuma.
La combustión de productos derivados del petróleo en el terraplén del parque de tanques se elimina mediante el suministro inmediato de espuma.
Durante la combustión de los productos del petróleo, su punto de ebullición (ver Tabla 69) aumenta gradualmente debido a la destilación fraccionada en curso, en relación con la cual también aumenta la temperatura de la capa superior.
| K Diagrama de un sistema de suministro de agua contra incendios para enfriar un tanque en llamas a través de un anillo de riego. |
Al quemar aceite en el tanque, la parte superior de la correa superior del tanque está expuesta a la llama. Cuando se quema aceite a un nivel más bajo, la altura del lado libre del tanque en contacto con la llama puede ser significativa. En este modo de combustión, el depósito puede colapsar. El agua de las boquillas de fuego o de los anillos de riego estacionarios, que cae sobre la parte exterior de las paredes superiores del tanque, los enfría (Fig.15.1), evitando así un accidente y el derrame de hidrocarburos en el terraplén, creando condiciones más favorables para el uso de espuma aire-mecánica.
Los resultados del estudio de la combustión de productos petrolíferos y sus mezclas son interesantes.
Su temperatura durante la combustión de productos petrolíferos es: gasolina 1200 C, queroseno de tractor 1100 C, combustible diesel 1100 C, petróleo crudo 1100 C, fuel oil 1000 C. Al quemar madera en pilas, la temperatura de la llama turbulenta alcanza 1200-1300 C.
En los últimos 15 años se han llevado a cabo estudios particularmente amplios en el campo de la física de la combustión de productos petrolíferos y su extinción en el Instituto Central de Investigación de Defensa contra Incendios (TsNIIPO), el Instituto de Energía de la Academia de Ciencias de la URSS (ENIN) y varios otros institutos de investigación y educación.
Un ejemplo de catálisis negativa es la supresión de la combustión de productos del petróleo con la adición de hidrocarburos halogenados.
El agua promueve la formación de espuma y emulsiones durante la combustión de productos derivados del petróleo con un punto de inflamación de 120 C y superior. La emulsión, que cubre la superficie del líquido, lo aísla del oxígeno del aire y también evita el escape de vapores.
| Tasa de combustión de gases de hidrocarburos licuados en tanques isotérmicos. |
La combustión de gases de hidrocarburos licuados en tanques isotérmicos no difiere de la combustión de productos petrolíferos. La velocidad de combustión en este caso puede calcularse mediante la fórmula (13) o determinarse experimentalmente. La peculiaridad de la combustión de gases licuados en condiciones isotérmicas es que la temperatura de toda la masa de líquido en el tanque es igual al punto de ebullición a presión atmosférica. Para hidrógeno, metano, etano, propano y butano, estas temperaturas son, respectivamente, - 252, - 161, - 88, - 42 y 0 5 C.
| Diagrama de instalación del generador GVPS-2000 en el tanque. |
La investigación y la práctica de la extinción de incendios han demostrado que para detener la combustión de un producto petrolífero, la espuma debe cubrir completamente toda su superficie con una capa de cierto espesor. Todas las espumas con una tasa de expansión baja son ineficaces para extinguir incendios de productos petrolíferos en tanques en el nivel más bajo de inundación. La espuma, que cae desde una gran altura (6 - 8 m) sobre la superficie del combustible, se sumerge y se envuelve en una película de combustible, se quema o se colapsa rápidamente. Solo se puede arrojar espuma con una multiplicidad de 70 a 150 en un tanque de combustión con chorros con bisagras.
| El fuego se rompe. |