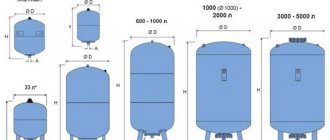
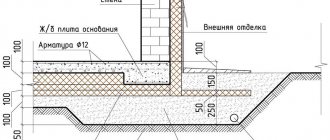
Einer der vielen physikochemischen Prozesse, die sowohl in der Industrie als auch im Alltag breite Anwendung gefunden haben, ist die Elektrolyse - die Auswahl der Elektroden auf den Oberflächen von Elektroden, die an eine Stromquelle angeschlossen sind, die in einer Lösung oder Schmelze angeordnet ist, deren Bestandteile (reines Metall - Aluminium, Kupfer, Gas usw.). Die Hauptinstallation, in der dieser Prozess stattfindet, ist ein Elektrolyseur.

Elektrolyseur
Was ist ein Elektrolyseur?
Ein Elektrolyseur ist eine spezielle Anlage, mit der seine Bestandteile von einer Lösung oder Schmelze getrennt werden.
Die Hauptmerkmale des Elektrolyseurs sind:
- Die Betriebsspannung für eine Elektrode reicht von 1,8 bis 2,0 V;
- Stromstärke - Für den normalen Verlauf des Elektrolyseprozesses wird den Elektroden ein Strom mit einem Wert dieser Eigenschaft von 5 bis 10 A zugeführt.
- Anzahl der Elektroden - Die minimale Anzahl der Elektroden beträgt 2, die maximale Anzahl ist durch die Größe der Anlage selbst und ihren Zweck begrenzt.
- Abmessungen der Elektroden - nicht Kohlenstoffstäbe werden als Elektroden verwendet, sondern Metallplatten, deren Größe durch den Zweck der Installation bestimmt wird, die Strom-Spannungs-Charakteristik des den Platten zugeführten Stroms;
- Abstand zwischen entgegengesetzt geladenen Elektrodenoberflächen - Der Mindestabstand zwischen den Elektrodenplatten muss mindestens 1,5 mm betragen.
- Elektrodenmaterial - In modernen Elektrolyseuren wird Edelstahlblech mit Nickel als Material für Anode und Kathode verwendet.
Ein weiteres wichtiges Merkmal einer Elektrolyseanlage ist die Verwendung von Katalysatoren.
Solche Installationen werden für folgende Zwecke verwendet:
- Erhalten eines Sauerstoffgases, bestehend aus einem Gemisch aus Wasserstoff und Sauerstoff (Browns Gas);
- Isolierung von reinem Aluminium, Magnesium, Zink aus ihren Salzschmelzen;
- Reinigung von Wasser aus darin gelösten Salzen und Verunreinigungen;
- Aufbringen einer dünnen Schicht aus Nickel und Zink, die Korrosion auf der Oberfläche von Metallteilen verhindert;
- Desinfektion von Lebensmitteln;
- Reinigung von Abwasser aus gelösten Salzen von Schwermetallen und anderen schädlichen Substanzen.
Wichtig! Platinelektroden aus gewöhnlichem Eisen werden in Elektrolyseanlagen seltener verwendet als aus Edelstahl, da sie schneller oxidieren und unbrauchbar werden.
Selbstgemachter Elektrolyseur
Jeder kann mit seinen eigenen Händen einen Elektrolyseur herstellen. Für den Montageprozess der gängigsten Konstruktion werden folgende Materialien benötigt:
- Edelstahlblech (die besten Optionen sind ausländische AISI 316L oder unsere 03X16H15M3);
- Schrauben М6х150;
- Unterlegscheiben und Muttern;
- transparente Röhre - Sie können eine Wasserwaage verwenden, die für Bauzwecke verwendet wird.
- mehrere Fischgrätenbeschläge mit einem Außendurchmesser von 8 mm;
- Kunststoffbehälter mit einem Volumen von 1,5 Litern;
- ein kleiner Filter, der Leitungswasser filtert, zum Beispiel ein Filter für Waschmaschinen;
- Rückschlagventil.
Montageprozess
Sammeln Sie den Elektrolyseur mit Ihren eigenen Händen gemäß den folgenden Anweisungen:
- Zunächst müssen Sie das Edelstahlblech markieren und anschließend in identische Quadrate sägen. Das Sägen kann mit einem Winkelschleifer (Winkelschleifer) erfolgen. Eine der Ecken in solchen Quadraten muss in einem Winkel geschnitten werden, um die Platten korrekt zu sichern.
- Als nächstes müssen Sie ein Loch für den Bolzen auf der Seite der Platte bohren, die dem Eckensägenschnitt gegenüberliegt.
- Das Anschließen der Platten sollte der Reihe nach erfolgen: eine Platte auf "+", die nächste auf "-" und so weiter;
- Zwischen den unterschiedlich geladenen Platten sollte sich ein Isolator befinden, der als Röhre von der Wasserwaage fungiert.Es sollte in Ringe geschnitten werden, die in Längsrichtung geschnitten werden sollten, um Streifen mit einer Dicke von 1 mm zu erhalten. Dieser Abstand zwischen den Platten reicht für eine gute Gasentwicklung während der Elektrolyse aus;
- Die Platten werden mit Unterlegscheiben wie folgt aneinander befestigt: Eine Unterlegscheibe sitzt auf dem Bolzen, dann eine Platte, dann drei Unterlegscheiben nach einer Platte und so weiter. Günstig geladene Platten werden in einem Spiegelbild von negativ geladenen Blättern angeordnet. Dadurch kann verhindert werden, dass die gesägten Kanten die Elektroden berühren.


Platten der Elektrolyseanlage zusammengebaut
- Wenn Sie die Platten zusammenbauen, sollten Sie sie gleichzeitig isolieren und die Muttern festziehen.
- Außerdem muss jede Platte mit einem Ring versehen sein, um sicherzustellen, dass kein Kurzschluss vorliegt.
- Ferner muss die gesamte Baugruppe in eine Plastikbox gelegt werden;
- Danach sollten Sie die Stellen hervorheben, an denen die Schrauben die Wände des Behälters berühren und an denen Sie zwei Löcher bohren. Wenn die Schrauben nicht in den Behälter passen, müssen sie mit einer Bügelsäge geschnitten werden.
- Dann werden die Schrauben mit Muttern und Unterlegscheiben festgezogen, um die Struktur dicht zu halten.


Platten in einen Plastikbehälter gelegt
- Nach den durchgeführten Schritten müssen Sie Löcher in den Behälterdeckel bohren und die Armaturen in diese einsetzen. Die Undurchlässigkeit kann in diesem Fall sichergestellt werden, indem die Fugen mit Dichtungsmitteln auf Silikonbasis abgedichtet werden.
- Ein Sicherheitsventil und ein Filter in der Struktur befinden sich am Auslass des Gases und dienen als Mittel zur Kontrolle einer übermäßigen Ansammlung von Gas, was zu schlechten Ergebnissen führen kann.
- Die Elektrolyseeinheit ist zusammengebaut.
Die letzte Stufe ist ein Test, der auf ähnliche Weise durchgeführt wird:
- Füllen des Behälters mit Wasser bis zur Markierung der Schrauben für Befestigungselemente;
- Anschließen der Stromversorgung an das Gerät;
- Verbindung zum Anschlussstück des Rohres, dessen gegenüberliegendes Ende ins Wasser abgesenkt ist.
Wenn der Anlage ein schwacher Strom zugeführt wird, ist die Freisetzung von Gas durch das Rohr fast nicht wahrnehmbar, es ist jedoch möglich, es vom Inneren des Elektrolyseurs aus zu beobachten. Durch Erhöhen des Wechselstroms durch Zugabe eines alkalischen Katalysators zum Wasser kann die Ausbeute der gasförmigen Substanz signifikant erhöht werden.
Der hergestellte Elektrolyseur ist in der Regel ein wichtiger Bestandteil vieler Geräte, beispielsweise eines Wasserstoffbrenners.


das Aussehen eines Wasserstoffbrenners, dessen Basis als selbstgebauter Elektrolyseur angesehen wird
Wenn Sie die Typen, Schlüsseleigenschaften, Geräte und Funktionsprinzipien von Ioneninstallationen kennen, können Sie die korrekte Montage einer selbst hergestellten Struktur durchführen, die in einer Vielzahl von Alltagssituationen ein hervorragender Assistent ist: vom Schweißen und Einsparen des Kraftstoffverbrauchs von Kraftfahrzeugen bis hin zu die Funktionsweise von Heizungssystemen.
Gerät und Funktionsprinzip
Kathode und Anode
Die einfachste Elektrolyseanlage besteht aus mehreren "Zellen", von denen jede Folgendes umfasst:
- 2 Plattenelektroden - Kathode (negativ) und Anode (positiv);
- Eine Gummidichtung um den Umfang zweier benachbarter unterschiedlicher Elektroden.
Die äußeren Zellen sind mit speziellen Rohren ausgestattet, durch die die entstehenden Gase abgelassen werden.
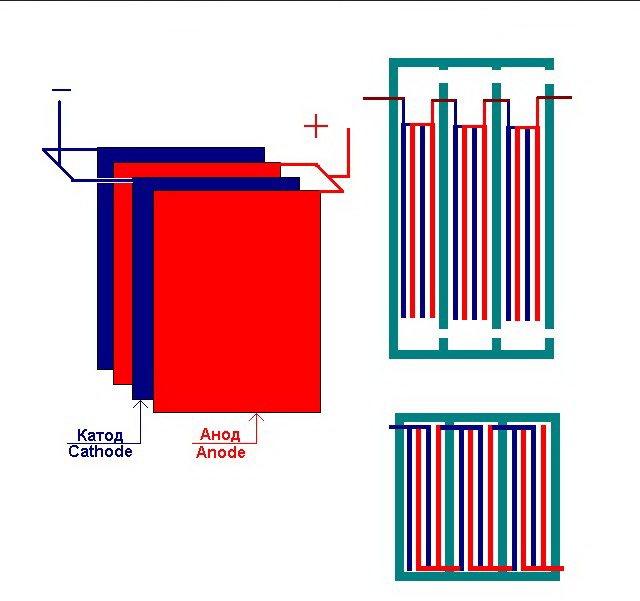

Mehrere miteinander verbundene "Zellen" der Elektrolyseanlage
Der Elektrolyseur kann 1 bis 30-40 oder mehr solcher "Zellen" enthalten, wobei die gleichnamigen Platten in Reihe geschaltet sind.
Wichtig! Bei Verwendung von Netzteilen mit Wechselstrom werden zusätzlich Gleichrichter verwendet, von denen der einfachste eine Diodenbrücke ist.
Eine solche Installation funktioniert wie folgt:
- In den Raum zwischen den Elektroden wird destilliertes Wasser mit darin gelöstem Alkali oder gewöhnlichem Backpulver gegossen;
- Eine Spannung von 1,8 bis 2,0 V wird von der Stromversorgung an die Elektroden aller Zellen der Anlage angelegt;
- Infolge des Elektrolyseprozesses werden Anionen (positiv geladene Ionen) einer in Wasser gelösten Substanz von der negativ geladenen Kathode angezogen, wodurch ein dünner Natriumfilm darauf gebildet wird;
- An einer positiv geladenen Anode kommt es zur Zerstörung von Wassermolekülen mit jeweils 2 Wasserstoffatomen und 1 Sauerstoffatom;
- Das durch die Abzweigrohre freigesetzte Sprenggas tritt in den dafür vorgesehenen Behälter ein.
Die Intensität des Elektrolyseprozesses hängt von der Spannungs- und Stromstärke ab - bei niedrigen Werten dieser Eigenschaften läuft der Prozess nicht ab. Wenn die Stromquelle einen Strom mit zu hohen Werten der Strom-Spannungs-Kennlinie liefert, ist die in den Elektrolyseur gegossene Lösung sehr heiß und kocht weg.
Debuggen und Testen des Geräts
Dann muss festgestellt werden, wo die Schrauben die Wände des Kastens berühren, und an diesen Stellen zwei Löcher gebohrt werden. Wenn sich ohne ersichtlichen Grund herausstellt, dass die Schrauben nicht in den Behälter passen, sollten sie es tun Mit Muttern abschneiden und festziehen... Jetzt müssen Sie die Abdeckung herausbohren und die Gewindeanschlüsse dort von beiden Seiten einführen. Um die Undurchlässigkeit sicherzustellen, sollte die Verbindung mit einem Dichtungsmittel auf Silikonbasis abgedichtet werden.
Nachdem Sie Ihren eigenen Elektrolyseur mit Ihren eigenen Händen zusammengebaut haben, sollten Sie ihn testen. Schließen Sie dazu das Gerät an eine Stromquelle an. Füllen Sie die Schrauben mit WasserSetzen Sie den Deckel auf, indem Sie ein Rohr an die Armatur anschließen und das gegenüberliegende Ende des Rohrs ins Wasser absenken. Wenn der Strom schwach ist, ist der Strom im Inneren des Elektrolyseurs sichtbar.
Erhöhen Sie schrittweise den Strom in Ihrem hausgemachten Gerät. Destilliertes Wasser leitet Elektrizität nicht gut, da es keine Salze oder Verunreinigungen enthält. Zur Herstellung des Elektrolyten muss dem Wasser Alkali zugesetzt werden. Dazu müssen Sie Natriumhydroxid (in den Pfeifenreinigern vom Typ "Mole" enthalten) einnehmen. Ein Sicherheitsventil ist erforderlich, um zu verhindern, dass sich eine angemessene Menge Gas ansammelt.
- Es ist besser, destilliertes Wasser und Soda als Katalysator zu verwenden.
- Sie sollten etwas Backpulver mit vierzig Teilen Wasser mischen. Die Wände an den Seiten bestehen am besten aus Acrylglas.
- Die Elektroden bestehen am besten aus Edelstahl. Es ist sinnvoll, Gold für Teller zu verwenden.
- Verwenden Sie für die Unterlage durchscheinendes PVC. Sie können 200 mal 160 Millimeter groß sein.
- Sie können Ihren eigenen Elektrolyseur verwenden, um Lebensmittel zu kochen, um Benzin in Autos und in den meisten Fällen vollständig zu verbrennen.
Trockenelektrolyseure werden hauptsächlich für Maschinen verwendet. Der Generator erhöht die Leistung des Verbrennungsmotors. Wasserstoff entzündet sich viel schneller als flüssiger Kraftstoff und erhöht die Kraft des Kolbens. Zusätzlich zu Mole können Sie Mister Muscle, Ätznatron und Backpulver einnehmen.
Der Generator arbeitet nicht mit Trinkwasser. Es ist besser, Strom so anzuschließen: die erste und die letzte Platte - Minus und auf der Platte in der Mitte - Plus. Je größer die Fläche der Platten und je stärker der Strom ist, desto mehr Gas wird freigesetzt.
Arten von Elektrolyseuren
DIY Punktschweißen für Batterien
Je nach Ausführung und Funktionsweise gibt es 5 Arten von Elektrolyseanlagen.
Trocken
Diese Elektrolyseure bestehen aus Plattenelektroden, die durch abgedichtete Gummidichtungen getrennt sind. Oft werden die "Zellen" der Anlage zusätzlich in einem versiegelten Gehäuse untergebracht.
Durch Elektrolyse entstehender Wasserstoff und Sauerstoff werden durch spezielle Abzweigrohre am Ende des Körpers oder an den äußersten Platten der Anlage entfernt.
Fließend
Elektrolyseanlagen dieses Typs haben das folgende Gerät:
- Ein Elektrolysebad (Körper) mit zwei Düsen, durch die einer Elektrolyt zugeführt wird, durch das zweite wird das durch die Elektrolyse gebildete Sprenggas abgegeben;
- Plattenelektroden durch Abstandshalter getrennt;
- Ein Tank mit Elektrolyt, der über dem Gehäuse mit Elektroden angeordnet und über Schläuche mit den Abzweigrohren des Elektrolysebades der Anlage verbunden ist und im oberen Teil ein Abzweigrohr mit einem Gasventil aufweist.
Während des Betriebs einer solchen Vorrichtung tritt das durch das Abzweigrohr und den Schlauch austretende Gas mit dem Elektrolyten in den Tank ein und verlässt die Anlage durch Erzeugen eines bestimmten Drucks durch das Ventil am Abzweigrohr.
Membran
Die Elektrolysezellen solcher Anlagen bestehen aus zwei Elektroden, die durch eine dünne Membran getrennt sind, durch die Elektrolyseprodukte hindurchtreten und die Elektroden voneinander trennen können.
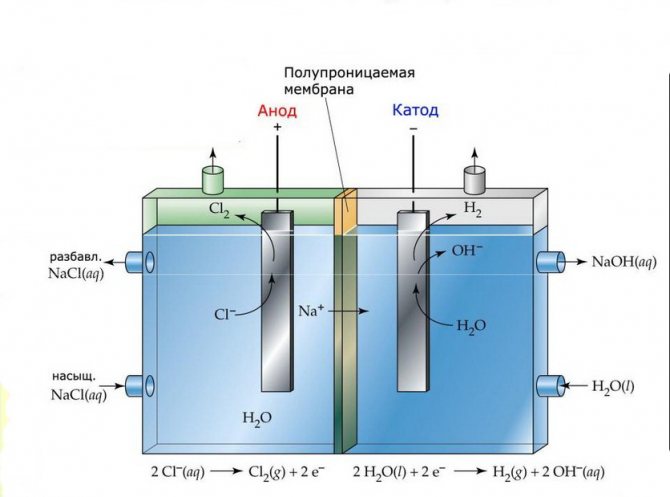

Membranelektrolyseanlage
Membran
Elektrolyseanlagen dieses Typs bestehen aus einem "U" -förmigen Kolben mit zwei eingesetzten Elektroden und 2-3 undurchlässigen Membranen. Ähnliche Elektrolyseure werden zur getrennten Herstellung von reinem Wasserstoff und Sauerstoff verwendet.
Alkalisch
Im Gegensatz zu anderen Modellen von Elektrolyseuren wird bei diesen eine Alkalilösung als Elektrolyt verwendet - Ätznatron (Natriumhydroxid), das nicht nur eine zusätzliche Quelle für Wasserstoff und Sauerstoff, sondern auch ein Katalysator für die Elektrolyse ist.
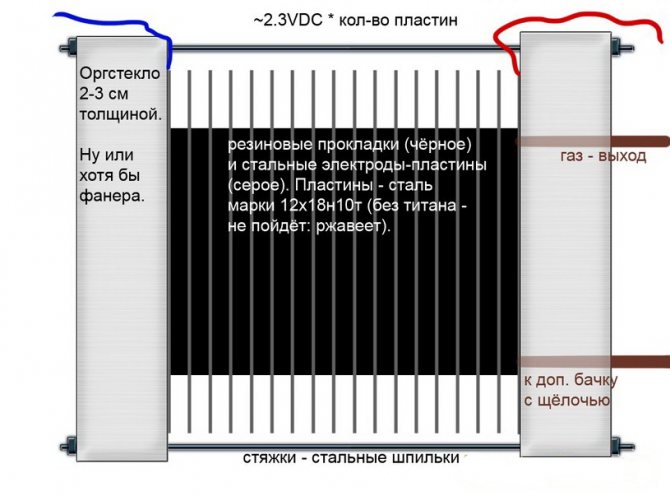

Alkalischer Elektrolyseurkreis
Solche Installationen ermöglichen im Gegensatz zu Analoga anderer Typen die Verwendung billigerer Elektroden aus gewöhnlichem Eisen.
Machen Sie den Elektrolyseur mit Ihren eigenen Händen
Sicherlich kennen Sie den Elektrolyseprozess aus dem Lehrplan der Grundschule. Dies ist der Fall, wenn 2 polare Elektroden unter Strom in Wasser gestellt werden, um Metalle oder Nichtmetalle in ihrer reinen Form zu erhalten. Ein Elektrolyseur wird benötigt, um Wassermoleküle in Sauerstoff und Wasserstoff zu zersetzen. Der Elektrolyseur teilt als Teil wissenschaftlicher Mechanismen Moleküle in Ionen.
Es gibt zwei Arten dieses Geräts:
- Trockenelektrolyseur (dies ist eine vollständig geschlossene Zelle);
- Nasselektrolyseur (dies sind zwei Metallplatten, die in einen Wasserbehälter gegeben werden).
Dieses Gerät ist in Bezug auf das Gerät einfach, was es möglich macht Verwenden Sie auch zu Hause... Elektrolyseure teilen die Elektrolyseladungen der Atome der Moleküle in geladene Atome auf.
In unserem Fall teilt es Wasser in positiven Wasserstoff und negativen Sauerstoff. Um dies zu tun, ist eine große Energiemenge erforderlich, und um die erforderliche Energie weniger zu nutzen, wird ein Katalysator verwendet.
Elektrolyseur zur Wasserstoffproduktion
Erdungsberechnung
Um den einfachsten Elektrolyseur mit Ihren eigenen Händen zusammenzubauen, können Sie die in der Abbildung gezeigte Zeichnung verwenden.
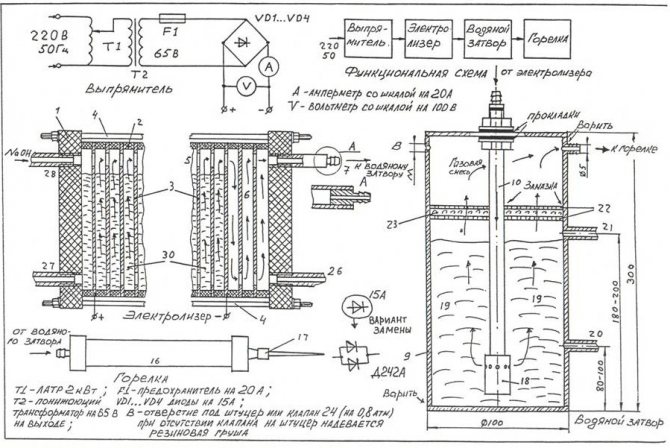

Zeichnung des einfachsten hausgemachten Elektrolyseurs
Beachten Sie! Ein Elektrolyseur ist eine ziemlich gefährliche Anlage, bei der während des Betriebs in großen Mengen angesammeltes Sauerstoffwasserstoffgas eine schwere Explosion verursachen kann. Das Gerät darf nicht in der Nähe von offenen Feuerquellen und Heizgeräten aufgestellt werden.
DIY Elektrolyseur für ein Auto
Um die Verbrennung von Kraftstoff in einem Automotor zu verbessern, wird häufig ein Elektrolyseur zusammengebaut, der aus einem Gehäuse aus einer alten Batterie mit eingelegten Edelstahlplatten und zwei Düsen besteht, von denen eine mit einem mit Elektrolyt gefüllten Tank verbunden ist, der zweite ist verbunden mit einem Luftzufuhrschlauch zum Motor (genauer gesagt mit einer Wellung vom Lufteinlass zum Luftfilter).
Ein solcher hausgemachter fließender Elektrolyseur wird über ein Relais und eine 10-A-Sicherung aus der Autobatterie gespeist.
Wir erstellen ein Gerät mit unseren eigenen Händen
Das Gerät für diesen Vorgang kann von Hand gemacht werden.
Dafür benötigen Sie:
- Edelstahlblech;
- Schrauben M6 x 150;
- Unterlegscheiben;
- Nüsse;
- Transparente Röhre;
- Verbindungselemente mit beidseitigem Gewinde;
- Eineinhalb Liter Plastikbehälter;
- Wasserfilter;
- Rückschlagventil auf Wasser.
Eine ausgezeichnete Option für Edelstahl ist AISI 316L eines ausländischen Herstellers oder 03X16H15M3 eines Herstellers aus unserem Land. Es ist absolut nicht nötig, Edelstahl zu kaufen, Sie können den alten nehmen. 50 bis 50 Zentimeter sind genug für Sie.
"Warum Edelstahl selbst nehmen?" - du fragst. Da das gebräuchlichste Metall korrodiert. Edelstahl verträgt Alkalien besser. Sollte skizzieren Sie das Blatt so, dass es in 16 ähnliche Quadrate unterteilt wird... Sie können es mit einem Winkelschleifer schneiden. Schneiden Sie in jedes Quadrat eine der Ecken.
Bohren Sie auf der anderen Seite und gegenüber der gegenüberliegenden Ecke von der abgesägten Ecke ein Loch für einen Bolzen, der die Platten zusammenhält. Der Elektrolyseur hört nicht auf, so zu arbeiten:t Plattenstrom fließt zur Platte - und Wasser zersetzt sich in Sauerstoff und Wasserstoff. Dank dessen brauchen wir eine gute und negative Platte.
Die Platten müssen abwechselnd angeschlossen werden: Plus-Minus-Plus-MinusMit einer ähnlichen Methode wird es einen starken Strom geben. Um die Platten einzeln zu isolieren, wird ein Rohr verwendet. Ein Ring wird aus der Ebene geschnitten. Durch das Schneiden erhalten wir einen Millimeter dicken Streifen. Dieser Abstand ist für die Gasherstellung korrekter.
Die Platten sind mit Unterlegscheiben miteinander verbunden: Wir setzen eine Unterlegscheibe auf den Bolzen, dann eine Platte und drei Unterlegscheiben, dann wieder eine Platte und so weiter. Auf dem Plus und Minus müssen acht Platten gepflanzt werden. Wenn alles richtig gemacht ist, berühren die Schnitte der Platten die Elektroden nicht.
Dann müssen Sie die Muttern festziehen und die Platten isolieren. Dann legen wir die Struktur in einen Plastikbehälter.
Übersicht der Hersteller von Elektrolyseuren
Die Hauptproduzenten von Elektrolyseuren sind sowohl inländische Unternehmen (RUSAL, NPF RutTech, JSC Uralkhimmash) als auch deren ausländische Wettbewerber - Teledyne Energy Systems, Inc (USA), Hydrogenics Corp. (Belgien).
Somit ist der Elektrolyseur eine ziemlich einfache und funktionsreiche Anlage zur Erzeugung von Sauerstoffgas, das in Zukunft als Brennstoff für Verbrennungsmotoren und Heizkessel verwendet werden soll.
Heimwerkerelektrolyse
Als ich klein war, wollte ich immer etwas selbst machen, mit meinen eigenen Händen. Aber die Eltern (und andere nahe stehende Personen) haben dies in den meisten Fällen nicht zugelassen. Und ich habe damals (und bis jetzt sehe ich nichts) nichts Schlechtes gesehen, wenn kleine Kinder lernen wollen?
Natürlich habe ich diesen Artikel nicht geschrieben, um mich an Kindheitserfahrungen im Wunsch nach Selbstbildung zu erinnern. Zufällig stieß ich beim Surfen im Internet auf eine solche Frage. Ein kleiner Bomberjunge stellte Fragen, wie man zu Hause Elektrolyse macht. Stimmt, ich habe ihm nicht geantwortet, weil dieser Junge die schmerzlich verdächtige Mischung elektrolysieren wollte? Ich beschloss, dass ich nicht weiter aus Sünde sagen würde, sondern mich selbst in Büchern umsehen würde. Aber vor nicht allzu langer Zeit, als ich wieder durch die Foren wanderte, sah ich eine ähnliche Frage von einem Lehrer an einer Chemieschule. Nach der Beschreibung zu urteilen, ist seine Schule so arm, dass sie keinen Elektrolyseur für 300 Rubel kaufen kann (will). Der Lehrer (was für ein Problem!) Konnte keinen Ausweg aus der daraus resultierenden Situation finden. Also habe ich ihm geholfen. Für diejenigen, die neugierig auf diese Art von hausgemachten Produkten sind, poste ich diesen Artikel auf der Website.
Tatsächlich ist der Produktionsprozess und die Verwendung unserer Selbstpalette sehr primitiv. Aber ich werde Ihnen zuerst über Sicherheit und dann über die Herstellung erzählen - im zweiten. Und der Punkt ist, dass es sich um einen Demonstrationselektrolyseur handelt und nicht um eine Industrieanlage. Aus diesem Grund ist es aus Sicherheitsgründen gut, es nicht über das Netzwerk, sondern über das Netzwerk mit Strom zu versorgen von AA-Batterien oder aus einer Batterie. Je höher die Spannung, desto schneller verläuft natürlich der Elektrolyseprozess. Für die visuelle Beobachtung von Gasblasen ist es jedoch recht genug 6 V., aber 220 ist schon übertrieben. Mit einer solchen Spannung kocht beispielsweise Wasser am schnellsten, und das ist nicht sehr sicher ... Nun, ich denke, Sie haben die Spannung herausgefunden?
Lassen Sie uns nun darüber sprechen, wo und unter welchen Bedingungen wir experimentieren werden. Das allererste, es sollte entweder freier Raum oder ein gut belüfteter Raum sein. Obwohl ich alles in einer Wohnung mit geschlossenen Fenstern gemacht habe und nichts wie? Zweitens wird das Experiment am besten an einem guten Tisch durchgeführt. Das Wort "gut" bedeutet, dass der Tisch stabil und besser schwer, starr und an der Bodenoberfläche befestigt sein muss. In diesem Fall muss die Tischdecke gegen aggressive Substanzen beständig sein. Fliesen von Fliesen sind übrigens perfekt dafür (obwohl leider nicht alle). Ein Tisch wie dieser wird nicht nur für diese Erfahrung nützlich sein. Allerdings habe ich alles auf einem gewöhnlichen Hocker gemacht? Drittens müssen Sie während des Experiments die Stromquelle (in meinem Fall die Batterien) nicht bewegen. Aus Gründen der Zuverlässigkeit ist es aus Gründen der Zuverlässigkeit am besten, sie sofort auf den Tisch zu legen und so zu befestigen, dass sie sich nicht bewegen. Glauben Sie mir, das ist bequemer, als sie regelmäßig mit Ihren Händen zu halten. Ich band einfach meine eigenen Batterien mit Klebeband an das erste harte Objekt, das ich sah. Viertens, die Gerichte, in denen wir experimentieren werden, lassen sie klein sein. Ein einfaches Glas passt oder ein Schnapsglas. Übrigens ist dies die optimalste Art, Gläser zu Hause zu verwenden, anstatt bei weiterer Verwendung Alkohol in sie zu gießen ...
Nun wollen wir uns speziell dem Gerät zuwenden. Es ist in der Abbildung dargestellt, aber im Moment werde ich kurz erklären, was und was.
Wir müssen einen einfachen Bleistift nehmen und den Baum mit einem gewöhnlichen Messer entfernen und eine ganze Mine aus dem Bleistift herausholen. Sie können jedoch eine Mine von einem Druckbleistift nehmen. Es gibt jedoch zwei Schwierigkeiten gleichzeitig. Der erste ist der übliche. Die Mine eines Druckbleistifts ist zu dünn, für uns ist dies einfach nicht für ein visuelles Experiment geeignet. Die zweite Schwierigkeit ist eine unverständliche Zusammensetzung der aktuellen Schiefer. Es fühlt sich an, als wären sie nicht aus Graphit, sondern aus etwas anderem. Im Allgemeinen war meine Erfahrung mit einem solchen "Blei" selbst bei einer Spannung von 24 V überhaupt nicht erfolgreich. Dank dessen musste ich einen guten holzigen einfachen Bleistift auswählen. Der resultierende Graphitstab wird für uns als Elektrode dienen. Wie Sie sich vorstellen können, benötigen wir zwei Elektroden. Dank dessen holen wir uns den zweiten Bleistift oder brechen einfach den vorhandenen Stab in zwei Teile. Ich habe das tatsächlich getan.
Mit jedem Draht, der zur Hand ist, wickeln wir die erste Elektrode (mit einem Ende des Drahtes) ein und verbinden diesen Draht mit dem Minus der Stromquelle (mit dem anderen Ende). Dann übernehmen wir die zweite Führung und machen dasselbe damit. Dafür benötigen wir einen zweiten Draht. In diesem Fall verbinden wir dieses Kabel mit dem Plus des Netzteils. Wenn Sie Probleme haben, den zerbrechlichen Graphitstab am Draht zu befestigen, können Sie die vorhandenen Werkzeuge wie Klebeband oder Klebeband verwenden. Wenn es nicht geklappt hat, die Spitze des Graphits mit dem Draht selbst zu umwickeln, und das Klebeband oder Isolierband keinen festen Kontakt hatte, versuchen Sie, das Kabel mit leitendem Kleber zu verkleben. Wenn Sie dies nicht haben, binden Sie zumindest die Leitung mit einem Faden an den Draht. Keine Angst, der Faden brennt bei solchen Spannungen nicht aus?
Für diejenigen, die nichts über Batterien und die einfachen Regeln für den Anschluss wissen, werde ich ein wenig erklären. Die Fingerbatterie erzeugt eine Spannung von 1,5 V. Auf dem Bild habe ich zwei ähnliche Batterien. Darüber hinaus sind sie miteinander verbunden allmählich - nacheinander, nicht parallel. Bei einer ähnlichen (seriellen) Verbindung wird die Endspannung aus der Spannung jeder Batterie summiert, dh für mich beträgt sie 1,5 + 1,5 = 3,0 V. Dies ist weniger als die zuvor angegebenen 6 Volt. Aber ich war zu faul, um noch ein paar Batterien zu kaufen. Prinzip Sie und so muss klar sein?
Beginnen wir mit dem Experiment. Zum Beispiel beschränken wir uns auf die Elektrolyse von Wasser.Erstens ist es sehr zugänglich (ich hoffe, dass der Leser dieses Artikels nicht in der Sahara lebt), und zweitens ist es harmlos. Außerdem werde ich zeigen, wie mit dem gleichen Gerät (Elektrolyseur) mit der gleichen Substanz (Wasser) zwei durchgeführt werden können verschiedene Erfahrung. Ich denke, dass Sie genug Fantasie haben, um eine Reihe ähnlicher Experimente mit anderen Substanzen zu entwickeln? Leitungswasser ist in der Regel für uns geeignet. Aber ich empfehle Ihnen, etwas mehr davon hinzuzufügen und zu salzen. Ein bisschen - Dies bedeutet eine kleine Prise, nicht einen ganzen Dessertlöffel. Das ist wichtig! Rühren Sie das Salz gut um, um sich aufzulösen. Wasser, das ein Dielektrikum in einem reinen Zustand ist, leitet Elektrizität perfekt. Wischen Sie zu Beginn des Experiments den Tisch von potenzieller Feuchtigkeit ab und stellen Sie dann die Stromquelle und ein Glas Wasser darauf.
Wir senken beide unter Spannung stehenden Elektroden ins Wasser. Stellen Sie gleichzeitig sicher, dass nur Graphit in das Wasser eingetaucht ist und der Draht selbst das Wasser nicht berühren darf. Der Beginn des Experiments kann sich verzögern. Die Zeit hängt von vielen Indikatoren ab: von der Zusammensetzung des Wassers, der Qualität der Drähte, der Qualität des Graphits und natürlich der Spannung der Stromquelle. Der Beginn meiner Reaktion verzögerte sich um einige Sekunden. An der Elektrode, die mit dem Plus der Batterien verbunden war, beginnt sich Sauerstoff zu entwickeln. An der mit dem Minus verbundenen Elektrode wird Wasserstoff freigesetzt. Es ist zu beachten, dass mehr Wasserstoffblasen vorhanden sind. Sehr kleine Blasen kleben um den Teil des Graphits, der in das Wasser getaucht ist. Dann beginnen einige der Blasen zu schweben.
Elektrode zu Beginn des Experiments. Es gibt noch keine Gasblasen. An der Elektrode, die mit dem Minuspol der Batterien verbunden ist, bildeten sich Wasserstoffblasen
Welche anderen Experimente kann es geben? Wenn Sie bereits genug mit Wasserstoff und Sauerstoff gespielt haben, fahren wir mit einem weiteren Experiment fort. Es ist interessanter, insbesondere für Heimforscher. Es ist insofern interessant, als man es nicht nur sehen, sondern auch riechen kann. In der Vergangenheit haben wir Sauerstoff und Wasserstoff erhalten, die meiner Meinung nach nicht sehr spektakulär sind. Und in einem anderen Experiment erhalten wir zwei Substanzen (übrigens nützlich im Alltag). Beenden Sie zu Beginn des Experiments das vorherige Experiment und trocknen Sie die Elektroden. Nehmen Sie nun Speisesalz (das Sie normalerweise im Küchenzimmer verwenden) und lösen Sie es in der Wassermasse auf. In diesem Fall keine geringe Menge. Tatsächlich ist eine anständige Menge Salz das einzige, was die zweite Erfahrung von der ersten unterscheidet. Nach dem Auflösen des Salzes können Sie den Versuch sofort wiederholen. Jetzt findet eine andere Reaktion statt. Auf einer guten Elektrode wird jetzt nicht Sauerstoff freigesetzt, sondern Chlor. Und negativ ist, dass auch Wasserstoff freigesetzt wird. Bei dem Glas, in dem sich die Salzlösung befindet, verbleibt nach längerer Elektrolyse Natriumhydroxid darin. Dies ist die bekannte Natronlauge, Alkali.
Chlor, Sie werden es riechen können. Für den besten Effekt empfehle ich jedoch eine Spannung von mindestens 12 V. Andernfalls können Sie das Aroma möglicherweise nicht spüren. Das Vorhandensein von Alkali (nach einer sehr langen Elektrolyse) im Glas kann auf verschiedene Arten überprüft werden. Am einfachsten und gewalttätigsten ist es, die Hand in das Glas zu legen. Ein ethnisches Omen sagt, dass, wenn ein brennendes Gefühl beginnt, Alkali im Glas ist. Ein intelligenterer und eindeutigerer Weg ist der Lackmustest. Wenn Ihre Schule so arm ist, dass sie nicht einmal in der Lage ist, einen Lackmus zu erwerben, werden Ihnen praktische Indikatoren helfen. Eine davon, wie sie sagen, kann als Tropfen Rübensaft dienen? Es ist jedoch durchaus möglich, nur ein wenig Fett in die Lösung zu tropfen. Soweit ich weiß, sollte die Verseifung stattfinden.
Für die sehr Neugierigen werde ich beschreiben, was tatsächlich während der Experimente passiert ist. Im ersten Versuch fand unter dem Einfluss eines elektrischen Stroms eine ähnliche Reaktion statt: 2 H2O >>> 2 H2 + O2 Beide Gase schwimmen natürlich vom Wasser an die Oberfläche. Übrigens können schwimmende Gase eingeschlossen werden. Wirst du es selbst schaffen?
In einem anderen Experiment war die Reaktion völlig anders.Es wurde auch durch elektrischen Strom ausgelöst, aber jetzt fungierte nicht nur Wasser, sondern auch Salz als Reagenzien: 4H2O + 4NaCl >>> 4NaOH + 2H2 + 2Cl2 Beachten Sie, dass die Reaktion in einem Überschuss an Wasser stattfinden muss. Um herauszufinden, welche Salzmenge als die größte angesehen wird, können Sie sie anhand der obigen Reaktion zählen. Sie können immer noch darüber nachdenken, wie Sie das Gerät verbessern oder welche anderen Experimente durchgeführt werden können. In der Tat ist es möglich, dass Natriumhypochlorit durch Elektrolyse erhalten werden kann. Unter Laborbedingungen wird es in den meisten Fällen erhalten, indem gasförmiges Chlor durch eine Natriumhydroxidlösung geleitet wird.