Estabilidade química
Considerando as propriedades químicas da gasolina, é necessário focar em quanto tempo a composição dos hidrocarbonetos permanecerá inalterada, uma vez que com um longo armazenamento, componentes mais leves desaparecem e o desempenho é muito reduzido.
Em particular, o problema é agudo se um combustível de grau superior (AI 95) foi obtido da gasolina com um número de octanas mínimo adicionando propano ou metano à sua composição. Suas propriedades anti-detonação são superiores às do isooctano, mas também se dissipam instantaneamente.
De acordo com o GOST, a composição química do combustível de qualquer marca deve permanecer inalterada por 5 anos, sujeita às regras de armazenamento. Mas, na verdade, muitas vezes até mesmo o combustível recém-adquirido já tem um número de octanas abaixo do especificado.
Os vendedores inescrupulosos são os culpados por isso, que adicionam gás liquefeito aos recipientes com combustível, cujo tempo de armazenamento expirou e o conteúdo não atende aos requisitos do GOST. Normalmente, diferentes quantidades de gás são adicionadas ao mesmo combustível para obter um número de octanas de 92 ou 95. A confirmação de tais truques é o cheiro pungente de gás no posto de gasolina.
Métodos de determinação do ponto de fulgor
Existe um método de cadinho aberto e fechado (recipiente para derivados de petróleo). As temperaturas obtidas diferem devido à quantidade de vapores acumulados.
O método do cadinho aberto inclui:
- Limpando a gasolina da umidade usando cloreto de sódio.
- Encher o cadinho até um certo nível.
- Aquecer o recipiente a uma temperatura 10 graus abaixo do resultado esperado.
- Ignição de um queimador de gás acima da superfície.
- No momento da ignição, o ponto de fulgor é registrado.
O método do cadinho fechado difere porque a gasolina no recipiente é constantemente misturada. Quando a tampa é aberta, o fogo é aceso automaticamente.
O aparelho de ponto de fulgor consiste nos seguintes componentes:
- aquecedor elétrico (potência de 600 watts);
- capacidade de 70 mililitros;
- agitador de cobre;
- ignitor elétrico ou a gás;
- termômetro.
Dependendo dos resultados, as substâncias inflamáveis são classificadas:
- especialmente perigoso (em um ponto de fulgor abaixo de -200C);
- perigoso (de -200C a + 230C);
- perigoso em temperaturas elevadas (de 230C a 610C).
Velocidade - Combustão - Combustível
Qual é o custo real de 1 litro de gasolina
A taxa de combustão do combustível aumenta muito se a mistura combustível estiver em movimento de vórtice (turbulento) intenso. Consequentemente, a intensidade da transferência turbulenta de calor pode ser muito maior do que a da difusão molecular.
A taxa de combustão do combustível depende de uma série de razões discutidas posteriormente neste capítulo e, em particular, da qualidade da mistura do combustível com o ar. A taxa de combustão do combustível é determinada pela quantidade de combustível queimado por unidade de tempo.
A taxa de combustão do combustível e, conseqüentemente, a taxa de liberação de calor são determinadas pelo tamanho da superfície de combustão. Pó de carvão com tamanho máximo de partícula de 300 - 500 mícrons tem uma superfície de combustão dezenas de milhares de vezes maior do que o combustível de grade de corrente classificada grossa.
A taxa de combustão do combustível depende da temperatura e pressão na câmara de combustão, aumentando com o seu aumento. Portanto, após a ignição, a taxa de combustão aumenta e torna-se muito alta no final da câmara de combustão.
A velocidade de combustão do combustível também é influenciada pela rotação do motor. Com o aumento do número de revoluções, a duração da fase é reduzida.
A turbulência do fluxo de gás aumenta drasticamente a taxa de combustão do combustível devido ao aumento da área da superfície de combustão e a velocidade de propagação da frente da chama com o aumento da taxa de transferência de calor.
Ao trabalhar com uma mistura pobre, a taxa de combustão é reduzida. Portanto, a quantidade de calor emitida pelos gases para as peças aumenta e o motor sobreaquece. Os sinais de uma mistura excessivamente pobre são flashes no carburador e no coletor de admissão.
A turbulência do fluxo de gás aumenta drasticamente a taxa de combustão do combustível devido ao aumento da área da superfície de combustão e a velocidade de propagação da frente da chama devido ao aumento da taxa de transferência de calor.
Os alcanos normais têm o número máximo de cetano, que caracteriza a taxa de combustão do combustível em um motor.
A composição da mistura de trabalho afeta muito a taxa de combustão do combustível no motor. Essas condições ocorrem em coeff.
A influência da qualidade do desenvolvimento do processo de combustão é determinada pela taxa de combustão do combustível na fase principal. Quando uma grande quantidade de combustível é queimada nesta fase, os valores de pz e Tz aumentam, a proporção de combustível de pós-combustão diminui durante o processo de expansão e o índice politrópico nz torna-se maior. Este desenvolvimento do processo é o mais favorável, uma vez que se consegue o melhor aproveitamento do calor.
No processo de trabalho do motor, o valor da taxa de combustão do combustível é muito importante. A taxa de combustão é entendida como a quantidade (massa) de combustível reagindo (queimando) por unidade de tempo.
Vários fenômenos gerais indicam que a taxa de combustão do combustível nos motores é bastante natural, não aleatória. Isso é indicado pela reprodutibilidade de ciclos mais ou menos inequívocos no cilindro do motor, o que, de fato, determina o funcionamento estável dos motores. Nos mesmos motores, a natureza prolongada da combustão é sempre observada com misturas pobres. O trabalho duro do motor, que ocorre em um alto índice de reações de combustão, é observado, via de regra, em motores a diesel sem compressor, e o trabalho suave - em motores com ignição por faísca elétrica. Isso indica que a formação e a ignição de misturas fundamentalmente diferentes causam uma mudança regular na taxa de combustão. Com o aumento da rotação do motor, a duração da combustão diminui com o tempo e, no ângulo de rotação do virabrequim, aumenta. As curvas cinéticas do curso da combustão em motores são de natureza semelhante às curvas cinéticas de uma série de reações químicas que não estão diretamente relacionadas aos motores e ocorrem em condições diferentes.
Os experimentos indicam a dependência da intensidade da transferência de calor radiante na taxa de combustão do combustível. Com a combustão rápida na raiz da tocha, as temperaturas mais altas se desenvolvem e a transferência de calor se intensifica. A não homogeneidade do campo de temperatura, junto com diferentes concentrações de partículas emissoras, leva à falta de homogeneidade do grau de escuridão da chama. Tudo isso cria grandes dificuldades para a determinação analítica da temperatura do radiador e do grau de emissividade do forno.
Com uma chama laminar (ver Seção 3 para mais detalhes), a taxa de combustão do combustível é constante e Q 0; o processo de combustão é silencioso. No entanto, se a zona de combustão for turbulenta, e este é o caso em consideração, então mesmo que o consumo de combustível seja constante em média, a taxa de combustão local muda com o tempo e para um elemento de pequeno volume Q.Q. A turbulência está continuamente perturbando a chama; a qualquer momento, a combustão é limitada por esta chama ou uma série de chamas, ocupando uma posição aleatória na zona de combustão.
Combustível gasoso
O combustível gasoso é uma mistura de vários gases: metano, etileno e outros hidrocarbonetos, monóxido de carbono, dióxido de carbono ou dióxido de carbono, nitrogênio, hidrogênio, sulfeto de hidrogênio, oxigênio e outros gases, bem como vapor d'água.
O metano (CH4) é o principal constituinte de muitos gases naturais. Seu conteúdo em gases naturais chega a 93 ... 98%. A combustão de 1 m3 de metano libera ~ 35.800 kJ de calor.
Os combustíveis gasosos também podem conter pequenas quantidades de etileno (C2H4). A combustão de 1 m3 de etileno dá ~ 59.000 kJ de calor.
Além de metano e etileno, os combustíveis gasosos também contêm compostos de hidrocarbonetos, como propano (C3H8), butano (C4H10), etc. A combustão desses hidrocarbonetos produz mais calor do que a combustão de etileno, mas sua quantidade é insignificante em gases combustíveis .
O hidrogênio (H2) é 14,5 vezes mais leve que o ar. A combustão de 1 m3 de hidrogênio libera ~ 10 800 kJ de calor. Muitos gases combustíveis, exceto o gás de forno de coque, contêm quantidades relativamente pequenas de hidrogênio. No gás de coqueria, seu conteúdo pode chegar a 50 ... 60%.
O monóxido de carbono (CO) é o principal componente combustível do gás de alto forno. A combustão de 1 m3 desse gás produz ~ 12.770 kJ de calor. Este gás é incolor, inodoro e altamente tóxico.
O sulfeto de hidrogênio (H2S) é um gás pesado com odor desagradável e altamente tóxico. Na presença de sulfeto de hidrogênio no gás, aumenta a corrosão das partes metálicas do forno e do gasoduto. O efeito prejudicial do sulfeto de hidrogênio é potencializado pela presença de oxigênio e umidade no gás. A combustão de 1 m3 de sulfeto de hidrogênio libera ~ 23.400 kJ de calor.
Os demais gases: CO2, N2, O2 e vapor d'água são componentes do lastro, pois com o aumento do conteúdo desses gases no combustível, o conteúdo de seus componentes combustíveis diminui. Sua presença leva a uma diminuição da temperatura de combustão do combustível. Um conteúdo de> 0,5% de oxigênio livre em combustíveis gasosos é considerado perigoso por razões de segurança.
Fervendo - gasolina
Número de octano composição da gasolina
A gasolina começa a ferver a uma temperatura relativamente baixa e continua muito intensamente.
O fim do ponto de ebulição da gasolina não é especificado.
O início de ebulição da gasolina é inferior a 40 C, o final é de 180 C, a temperatura de início da cristalização não é superior a 60 C. A acidez da gasolina não ultrapassa 1 mg / 100 ml.
O ponto de ebulição final da gasolina de acordo com GOST é 185 C, e o atual é 180 C.
O ponto de ebulição final da gasolina é a temperatura na qual uma porção padrão (100 ml) da gasolina testada é completamente destilada (fervida) do frasco de vidro em que foi colocada no refrigerador-receptor.
| Diagrama de instalação de estabilização. |
O ponto de ebulição final da gasolina não deve ultrapassar 200 - 225 C. Para as gasolinas de aviação, o ponto de ebulição final é muito mais baixo, chegando em alguns casos até 120 C.
MPa, o ponto de ebulição da gasolina é 338 K, sua massa molar média é 120 kg / kmol e o calor de vaporização é 252 kJ / kg.
O ponto de ebulição inicial da gasolina, por exemplo 40 para gasolina de aviação, indica a presença de frações leves e de baixo ponto de ebulição, mas não indica seu conteúdo. O ponto de ebulição da primeira fração de 10%, ou temperatura inicial, caracteriza as propriedades de partida da gasolina, sua volatilidade, bem como a tendência de formação de bujões de gás no sistema de abastecimento de gasolina. Quanto menor o ponto de ebulição da fração de 10%, mais fácil é dar partida no motor, mas também maior a possibilidade de formação de travas de gás, que podem causar interrupções no abastecimento de combustível e até mesmo desligar o motor. O ponto de ebulição muito alto da fração de partida dificulta a partida do motor em temperaturas ambientes baixas, o que leva a perdas de gasolina.
| Influência do ponto final do ponto de ebulição da gasolina no seu consumo durante a operação do veículo. Efeito da temperatura de destilação de 90% da gasolina sobre o número de octanas de gasolinas de várias origens. |
Uma diminuição no final do ponto de ebulição das gasolinas de reforma leva a uma deterioração em sua resistência à detonação. Pesquisa e cálculos econômicos são necessários para resolver este problema.De notar que, na prática estrangeira de vários países, estão actualmente a ser produzidas e utilizadas gasolinas para motores com um ponto de ebulição de 215 - 220 C.
| Influência do ponto final do ponto de ebulição da gasolina no seu consumo durante a operação do veículo. Influência da temperatura de destilação de 90% da gasolina no índice de octanas de gasolinas de várias origens. |
Uma diminuição no final do ponto de ebulição das gasolinas de reforma leva à deterioração de sua resistência à detonação. Pesquisas e cálculos econômicos são necessários para resolver esse problema. De notar que, na prática estrangeira de vários países, estão actualmente a ser produzidas e utilizadas gasolinas para motores com ponto de ebulição de 215 - 220 C.
Se o ponto de ebulição final da gasolina for alto, as frações pesadas contidas nela podem não evaporar e, portanto, não queimar no motor, o que aumentará o consumo de combustível.
A redução do ponto de ebulição final de gasolinas de destilação direta leva a um aumento em sua resistência à detonação. Gasolinas de corrida direta de baixa octanagem têm números de octanas de 75 e 68, respectivamente, e são usadas como componentes de gasolinas de motor.
Combustão - gasolina
Projeto e princípio de operação Bosch Motronic MED 7 sistema de injeção direta de gasolina
A combustão da gasolina, querosene e outros hidrocarbonetos líquidos ocorre na fase gasosa. A combustão só pode ocorrer quando a concentração de vapor de combustível no ar está dentro de certos limites, individuais para cada substância. Se uma pequena quantidade de vapores de combustível estiver contida no ar IB, a combustão não ocorrerá, bem como no caso em que há muito vapor de combustível e oxigênio insuficiente.
| Mudança de temperatura na superfície do querosene durante a extinção com espumas. Distribuição da temperatura no querosene antes do início da extinção (ae no final. |
Quando a gasolina queima, como se sabe, forma-se uma camada homotérmica, cuja espessura aumenta com o tempo.
Quando a gasolina queima, água e dióxido de carbono são formados. Isso pode servir como confirmação suficiente de que a gasolina não é um elemento?
Quando a gasolina, querosene e outros líquidos são queimados em tanques, o esmagamento do fluxo de gás em volumes separados e a combustão de cada um deles separadamente são especialmente claramente visíveis.
Quando a gasolina e o óleo são queimados em tanques de grande diâmetro, o caráter do aquecimento difere significativamente do descrito acima. Quando queimam, surge uma camada aquecida, cuja espessura aumenta naturalmente com o tempo e a temperatura é igual à temperatura na superfície do líquido. Abaixo dele, a temperatura do líquido cai rapidamente e se torna quase igual à temperatura inicial. A natureza das curvas mostra que, durante a combustão, a gasolina se divide em duas camadas - uma superior e uma inferior.
Por exemplo, queimar gasolina no ar é chamado de processo químico. Nesse caso, a energia é liberada, equivalente a aproximadamente 1300 kcal por 1 mol de gasolina.
A análise dos produtos da combustão da gasolina e dos óleos está se tornando extremamente importante, uma vez que o conhecimento da composição individual de tais produtos é necessário para o estudo dos processos de combustão no motor e para o estudo da poluição do ar.
Assim, quando a gasolina é queimada em tanques largos, até 40% do calor liberado como resultado da combustão é consumido para a radiação.
Tabela 76 mostra a taxa de queima de gasolina com aditivos de tetranitro-metano.
Experimentos descobriram que a velocidade de queima da gasolina na superfície do tanque é significativamente afetada por seu diâmetro.
| Alinhamento de forças e meios na extinção de incêndio no trecho. |
Com o auxílio do GPS-600, os bombeiros realizaram com sucesso a eliminação da queima da gasolina que derramava ao longo dos trilhos, garantindo o deslocamento dos operadores troncais até o local onde os tanques estavam acoplados.Depois de desconectá-los, com um pedaço de fio de contato, prenderam 2 tanques com gasolina ao carro de bombeiros e os puxaram para fora da zona de fogo.
| A taxa de aquecimento de óleos em tanques de vários diâmetros. |
Um aumento particularmente grande na velocidade de aquecimento do vento foi notado durante a queima de gasolina. Quando a gasolina estava queimando em um tanque de 2 64 m a uma velocidade do vento de 13 m / s, a taxa de aquecimento era de 9 63 mm / min, e a uma velocidade do vento de 10 m / s, a taxa de aquecimento aumentou para 17 1 mm / min.
Ponto de fulgor e outros parâmetros
A combustão do carvão é uma reação química de oxidação do carbono que ocorre em alta temperatura inicial com intensa liberação de calor. Agora é mais simples: o carvão combustível não pode inflamar como o papel; o pré-aquecimento a 370-700 ° C é necessário para a ignição, dependendo da marca do combustível.
Momento chave. A eficiência da combustão do carvão em uma fornalha ou caldeira doméstica de combustível sólido é caracterizada não pela temperatura máxima, mas pela completude da combustão. Cada molécula de carbono se combina com duas partículas de oxigênio no ar para formar o dióxido de carbono CO2. O processo se reflete na fórmula química.
Se você limitar a quantidade de oxigênio que entra (cubra o soprador, mude a caldeira TT para o modo de combustão lenta), em vez de CO2, monóxido de carbono CO é formado e emitido na chaminé, a eficiência de combustão diminuirá significativamente. Para alcançar alta eficiência, é necessário fornecer condições favoráveis:
- Carvões castanhos inflamam a uma temperatura de +370 ° C, pedra - 470 ° C, antracite - 700 graus. É necessário o pré-aquecimento da unidade de aquecimento com madeira (briquetes de serradura).
- O ar é fornecido à fornalha em excesso, o fator de segurança é 1,3-1,5.
- A combustão é sustentada pela alta temperatura das brasas que ficam na grelha. É importante garantir a passagem do oxigênio por toda a espessura do combustível, pois o ar passa pelo cinzeiro devido à tiragem natural da chaminé.
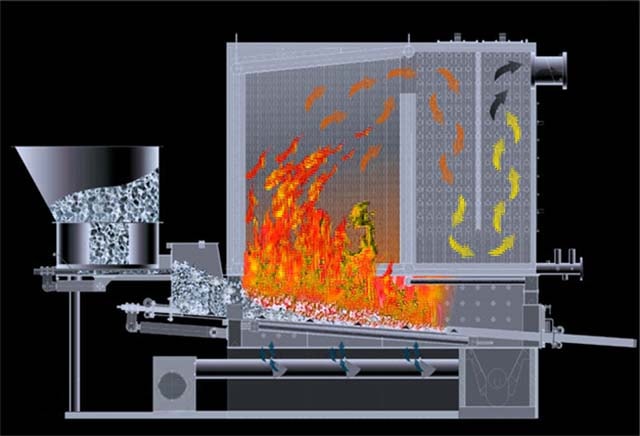
Comente. As únicas exceções são os fogões caseiros do tipo Bubafonya e as caldeiras cilíndricas para a combustão superior, onde o ar é alimentado na fornalha de cima para baixo.
A temperatura teórica de combustão e a transferência de calor específica de vários combustíveis são mostradas na tabela comparativa. É perceptível que, em condições ideais, qualquer combustível liberará calor máximo ao interagir com o volume de ar necessário.
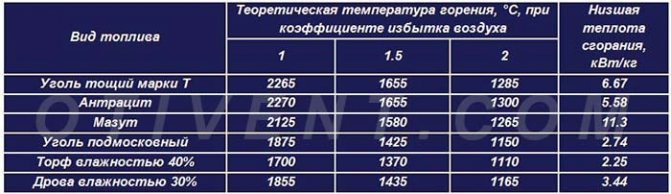

Na prática, não é realista criar tais condições, por isso o ar é fornecido com algum excesso. A temperatura real de combustão da lenhite em uma caldeira TT convencional é de 700 ... 800 ° C, pedra e antracito - 800 ... 1100 graus.
Se você exagerar na quantidade de oxigênio, a energia começará a ser gasta no aquecimento do ar e simplesmente voará para o cano, a eficiência da fornalha cairá visivelmente. Além disso, a temperatura do fogo pode chegar a 1500 ° C. O processo se assemelha a um fogo comum - a chama é grande, há pouco calor. Um exemplo de combustão eficiente de carvão com queimador de retorta em caldeira automática é apresentado no vídeo:
Temperatura - combustão - combustível
| Dependência do critério B da relação entre a área das fontes de calor e a área da oficina. |
A intensidade da irradiação do trabalhador depende da temperatura de combustão do combustível no forno, do tamanho do orifício de carregamento, da espessura das paredes do forno no orifício de carregamento e, finalmente, da distância a que o trabalhador está do carregamento orifício.
| As relações CO / CO e H2 / HO nos produtos da combustão incompleta do gás natural, em função do coeficiente de consumo de ar a. |
A temperatura 1L praticamente atingível é a temperatura de combustão do combustível em condições reais. Ao determinar seu valor, as perdas de calor para o meio ambiente, a duração do processo de combustão, o método de combustão e outros fatores são levados em consideração.
O excesso de ar afeta dramaticamente a temperatura de combustão do combustível.Assim, por exemplo, a temperatura real de combustão do gás natural com um excesso de 10% de ar é 1868 C, com um excesso de 20% de 1749 C e com um excesso de 100% de ar, diminui para 1167 C. Por outro lado , o pré-aquecimento do ar, indo para a combustão do combustível, aumenta a temperatura de sua combustão. Assim, ao queimar gás natural (1Max 2003 C) com ar aquecido a 200 C, a temperatura de combustão sobe para 2128 C, e quando o ar é aquecido a 400 C - até 2257 C.
| Diagrama geral do dispositivo do forno. |
Quando o ar e o combustível gasoso são aquecidos, a temperatura de combustão do combustível aumenta e, conseqüentemente, a temperatura do espaço de trabalho do forno também aumenta. Em muitos casos, é impossível atingir as temperaturas necessárias para um determinado processo tecnológico sem alto aquecimento do ar e do combustível gasoso. Por exemplo, a fundição de aço em fornos de lareira, para a qual a temperatura da tocha (fluxo de gases em combustão) no espaço de fusão deveria ser 1800 - 2000 C, seria impossível sem aquecer o ar e gás a 1000 - 1200 C. Quando aquecendo fornos industriais com combustível local de baixa caloria (lenha úmida, turfa, carvão marrom), seu trabalho sem aquecer o ar é muitas vezes impossível.
Pode-se verificar a partir desta fórmula que a temperatura de combustão do combustível pode ser aumentada aumentando seu numerador e diminuindo o denominador. A dependência da temperatura de combustão de vários gases na proporção de excesso de ar é mostrada na Fig.
O excesso de ar também afeta fortemente a temperatura de combustão do combustível. Assim, a produção de calor do gás natural com um excesso de ar de 10% - 1868 C, com um excesso de ar de 20% - 1749 C e com um excesso de 100% é igual a 1167 C.
Se a temperatura da junção quente for limitada apenas pela temperatura de combustão do combustível, o uso da recuperação torna possível aumentar a temperatura Тт aumentando a temperatura dos produtos de combustão e assim aumentar a eficiência geral do TEG.
O enriquecimento da explosão com oxigênio leva a um aumento significativo na temperatura de combustão do combustível. Como os dados do gráfico na Fig. 17, a temperatura teórica de combustão do combustível está associada ao enriquecimento da explosão com oxigênio por uma dependência, que é praticamente linear até o teor de oxigênio na explosão de 40%. Em graus mais elevados de enriquecimento, a dissociação dos produtos de combustão começa a ter um efeito significativo, em decorrência do qual as curvas de dependência da temperatura do grau de enriquecimento da explosão se desviam de linhas retas e se aproximam assintoticamente das temperaturas limites para um combustível. Assim, a dependência considerada da temperatura de combustão do combustível no grau de enriquecimento de oxigênio da explosão tem duas regiões - uma região de enriquecimento relativamente baixo, onde há uma dependência linear, e uma região de alto enriquecimento (acima de 40%), onde o aumento da temperatura tem um caráter decadente.
Um importante indicador termotécnico da operação do forno é a temperatura do forno, que depende da temperatura de combustão do combustível e da natureza do consumo de calor.
As cinzas do combustível, dependendo da composição das impurezas minerais, na temperatura de combustão do combustível podem ser fundidas em pedaços de escória. A característica da cinza do combustível dependendo da temperatura é dada na tabela. MAS.
O valor de tmaK na tabela. IV - З - temperatura calorimétrica (teórica) de combustão do combustível.
As perdas de calor pelas paredes dos fornos para o exterior (para o ambiente) reduzem a temperatura de combustão do combustível.
Combustão de combustível
A combustão de combustível é um processo de oxidação de componentes combustíveis que ocorre em altas temperaturas e é acompanhada pela liberação de calor. A natureza da combustão é determinada por muitos fatores, incluindo o método de combustão, o design do forno, a concentração de oxigênio, etc. Mas as condições do curso, a duração e os resultados finais dos processos de combustão dependem em grande parte da composição , características físicas e químicas do combustível.
Composição de combustível
Os combustíveis sólidos incluem carvão e carvão marrom, turfa, xisto betuminoso e madeira. Esses tipos de combustíveis são compostos orgânicos complexos formados principalmente por cinco elementos - carbono C, hidrogênio H, oxigênio O, enxofre S e nitrogênio N. O combustível também contém umidade e minerais não combustíveis, que formam cinzas após a combustão. A umidade e as cinzas são o lastro externo do combustível, enquanto o oxigênio e o nitrogênio são internos.
O principal elemento da parte combustível é o carbono, ele determina a liberação de maior quantidade de calor. No entanto, quanto maior a proporção de carbono em um combustível sólido, mais difícil será sua ignição. Durante a combustão, o hidrogênio libera 4,4 vezes mais calor do que o carbono, mas sua participação na composição dos combustíveis sólidos é pequena. O oxigênio, por não ser um elemento gerador de calor e aglutinador do hidrogênio e do carbono, reduz o calor de combustão, portanto é um elemento indesejável. Seu conteúdo é especialmente alto em turfa e madeira. A quantidade de nitrogênio nos combustíveis sólidos é pequena, mas é capaz de formar óxidos prejudiciais ao meio ambiente e ao homem. O enxofre também é uma impureza prejudicial, pois emite pouco calor, mas os óxidos resultantes levam à corrosão do metal das caldeiras e poluição da atmosfera.
Especificações do combustível e sua influência no processo de combustão
As características técnicas mais importantes do combustível são: calor de combustão, rendimento de substâncias voláteis, propriedades de resíduo não volátil (coque), teor de cinzas e teor de umidade.
Calor de combustão de combustível
O valor calorífico é a quantidade de calor liberada durante a combustão completa de uma unidade de massa (kJ / kg) ou volume de combustível (kJ / m3). Faça a distinção entre calor de combustão superior e inferior. O mais alto inclui o calor liberado durante a condensação dos vapores contidos nos produtos da combustão. Quando o combustível é queimado em fornos de caldeira, os gases de exaustão têm uma temperatura na qual a umidade está em estado de vapor. Portanto, neste caso, é utilizado um calor de combustão menor, que não leva em consideração o calor de condensação do vapor d'água.
A composição e o valor calorífico líquido de todos os depósitos de carvão conhecidos foram determinados e fornecidos nas características calculadas.
Liberação de matéria volátil
Quando o combustível sólido é aquecido sem acesso ao ar sob a influência da alta temperatura, primeiro o vapor d'água é liberado e, a seguir, ocorre a decomposição térmica das moléculas com a liberação de substâncias gasosas, chamadas de substâncias voláteis.
A liberação de substâncias voláteis pode ocorrer na faixa de temperatura de 160 a 1100 ° C, mas em média - na faixa de temperatura de 400-800 ° C. A temperatura de início da liberação dos voláteis, a quantidade e a composição dos produtos gasosos dependem da composição química do combustível. Quanto mais antigo quimicamente o combustível, menor será a liberação de voláteis e mais alta será a temperatura de início de sua liberação.
Os voláteis fornecem ignição mais precoce do material particulado e têm um efeito significativo na combustão do combustível. Combustíveis jovens - turfa, carvão marrom - inflamam facilmente, queimam rápida e quase completamente. Por outro lado, os combustíveis com baixo teor de voláteis, como o antracito, são mais difíceis de acender, queimam muito mais lentamente e não queimam completamente (com aumento da perda de calor).
Propriedades de resíduo não volátil (coque)
A parte sólida do combustível remanescente após a liberação dos voláteis, consistindo principalmente de carbono e uma parte mineral, é chamada de coque. O resíduo de coque pode ser, dependendo das propriedades dos compostos orgânicos incluídos na massa combustível: endurecido, endurecido (destruído pela exposição), pulverulento. Antracite, turfa e lenhite dão um resíduo pulverulento não volátil. A maioria dos carvões betuminosos são sinterizados, mas nem sempre fortemente. Resíduos pegajosos ou pulverulentos não voláteis fornecem carvão betuminoso com um rendimento muito alto de voláteis (42-45%) e com um rendimento muito baixo (menos de 17%).
A estrutura do resíduo de coque é importante na queima de carvão em fornos de grelha.Ao queimar em caldeiras, o desempenho do coque não é muito importante.
Conteúdo de cinzas
O combustível sólido contém a maior quantidade de impurezas minerais não combustíveis. Estes são principalmente argila, silicatos, pirita de ferro, mas óxido de ferro, sulfatos, carbonatos e silicatos de ferro, óxidos de vários metais, cloretos, álcalis, etc. também podem ser incluídos. A maioria deles cai durante a mineração na forma de rochas, entre as quais se encontram camadas de carvão, mas também há substâncias minerais que passaram para o combustível a partir dos formadores de carvão ou no processo de conversão de sua massa original.
Quando o combustível é queimado, as impurezas minerais passam por uma série de reações, resultando na formação de um resíduo sólido não combustível denominado cinza. O peso e a composição das cinzas não são idênticos ao peso e à composição das impurezas minerais do combustível.
As propriedades das cinzas desempenham um papel importante na organização da operação da caldeira e do forno. Suas partículas, levadas pelos produtos da combustão, desgastam as superfícies de aquecimento em altas velocidades e, em baixas velocidades, elas se depositam sobre elas, o que leva a uma deterioração na transferência de calor. As cinzas carregadas para a chaminé podem prejudicar o meio ambiente, para evitar isso é necessária a instalação de coletores de cinzas.
Uma propriedade importante das cinzas é sua fusibilidade; eles distinguem entre cinzas refratárias (acima de 1425 ° C), de ponto de fusão médio (1200-1425 ° C) e de baixo ponto de fusão (menos de 1200 ° C). A cinza que passou da fase de derretimento e se transformou em massa sinterizada ou fundida é chamada de escória. A característica de temperatura da fusibilidade da cinza é de grande importância para garantir o funcionamento confiável das superfícies do forno e da caldeira, a escolha correta da temperatura dos gases próximos a essas superfícies eliminará a escória.
Teor de umidade
A umidade é um componente indesejável do combustível, ela, junto com as impurezas minerais, é um lastro e reduz o conteúdo da parte combustível. Além disso, reduz o valor térmico, uma vez que é necessária energia adicional para sua evaporação.
A umidade do combustível pode ser interna ou externa. A umidade externa está contida nos capilares ou presa na superfície. Com a idade química, a quantidade de umidade capilar diminui. Quanto menores forem os pedaços de combustível, maior será a umidade da superfície. A umidade interna entra na matéria orgânica.
O teor de umidade no combustível reduz o calor de combustão e leva a um aumento no consumo de combustível. Ao mesmo tempo, os volumes de produtos de combustão aumentam, as perdas de calor com os gases de exaustão aumentam e a eficiência da unidade de caldeira diminui. A alta umidade no inverno leva ao congelamento do carvão, dificuldades de moagem e diminuição da fluidez.
Métodos de combustão de combustível, dependendo do tipo de forno
Os principais tipos de dispositivos de combustão:
- em camadas,
- câmara.
Fornos de camada destinam-se à combustão de combustível sólido granulado. Eles podem ser densos e fluidizados. Ao queimar em uma camada densa, o ar de combustão passa pela camada sem afetar sua estabilidade, ou seja, a gravidade das partículas em combustão supera a pressão dinâmica do ar. Quando queimadas em leito fluidizado, devido ao aumento da velocidade do ar, as partículas entram em estado de "ebulição". Nesse caso, ocorre a mistura ativa do oxidante e do combustível, o que intensifica a combustão do combustível.
NO fornos de câmara queimar combustível sólido pulverizado, bem como líquido e gasoso. Os fornos de câmara são subdivididos em ciclônicos e de alargamento. Durante a combustão do flare, as partículas de carvão não devem ter mais de 100 mícrons, elas queimam no volume da câmara de combustão. A combustão ciclônica permite um tamanho de partícula maior; sob a influência de forças centrífugas, elas são jogadas nas paredes do forno e queimam completamente em um fluxo turbulento em uma zona de alta temperatura.
Combustão de combustível. As principais etapas do processo
No processo de queima de combustível sólido, certas etapas podem ser distinguidas: aquecimento e evaporação da umidade, sublimação de voláteis e formação de resíduo de coque, combustão de voláteis e coque e formação de escória. Essa divisão do processo de combustão é relativamente arbitrária, pois embora essas etapas ocorram de forma sequencial, elas se sobrepõem parcialmente. Assim, a sublimação das substâncias voláteis começa antes da evaporação final de toda a umidade, a formação dos voláteis ocorre simultaneamente ao processo de sua combustão, assim como o início da oxidação do resíduo de coque antecede o fim da combustão dos voláteis, e o a pós-queima do coque também pode ocorrer após a formação de escória.
O tempo de fluxo de cada estágio do processo de combustão é amplamente determinado pelas propriedades do combustível. O estágio de combustão do coque é o mais longo, mesmo para combustíveis com alto rendimento volátil. Vários fatores operacionais e características de design do forno têm um impacto significativo na duração das etapas do processo de combustão.
1. Preparação do combustível antes da ignição
O combustível que entra na fornalha é aquecido e, como resultado, na presença de umidade, ele evapora e o combustível seca. O tempo necessário para aquecimento e secagem depende da quantidade de umidade e da temperatura na qual o combustível é fornecido ao dispositivo de combustão. Para combustíveis com alto teor de umidade (turfa, carvão marrom úmido), o estágio de aquecimento e secagem é relativamente longo.
O combustível é fornecido para fornos empilhados em uma temperatura próxima à temperatura ambiente. Somente no inverno, quando o carvão congela, sua temperatura é mais baixa do que na sala da caldeira. Para combustão em fornos de flare e vórtice, o combustível é submetido a trituração e moagem, acompanhada de secagem com ar quente ou gases de combustão. Quanto mais alta a temperatura do combustível que entra, menos tempo e menos calor são necessários para aquecê-lo até a temperatura de ignição.
A secagem do combustível na fornalha ocorre devido a duas fontes de calor: calor convectivo dos produtos da combustão e calor radiante de uma tocha, forro e escória.
Nos fornos de câmara, o aquecimento é realizado principalmente às custas da primeira fonte, ou seja, misturando os produtos da combustão ao combustível no ponto de sua entrada. Portanto, um dos requisitos importantes para o projeto de dispositivos para introdução de combustível no forno é garantir a sucção intensiva dos produtos de combustão. Uma temperatura mais alta na fornalha também contribui para um menor tempo de aquecimento e secagem. Para tanto, na queima de combustíveis com início de liberação de voláteis em altas temperaturas (mais de 400 ° C), as correias incendiárias são feitas em fornos de câmara, ou seja, fecham os tubos de blindagem com material refratário termo-isolante em a fim de reduzir sua percepção de calor.
Ao queimar combustível em uma cama, o papel de cada tipo de fonte de calor é determinado pelo projeto do forno. Em fornos com grelha de corrente, o aquecimento e a secagem são realizados principalmente pelo calor radiante da tocha. Em fornos com grelha fixa e fornecimento de combustível de cima, o aquecimento e a secagem ocorrem devido aos produtos de combustão que se movem através da camada de baixo para cima.
No processo de aquecimento a uma temperatura acima de 110 ° C, inicia-se a decomposição térmica das substâncias orgânicas que compõem os combustíveis. Os compostos menos fortes são aqueles que contêm uma quantidade significativa de oxigênio. Esses compostos se decompõem em temperaturas relativamente baixas com a formação de voláteis e um resíduo sólido, consistindo principalmente de carbono.
Combustíveis jovens na composição química, contendo muito oxigênio, apresentam baixa temperatura de início da liberação das substâncias gasosas e apresentam maior porcentagem delas. Combustíveis com baixo teor de compostos de oxigênio apresentam baixo rendimento de volatilidade e maior ponto de fulgor.
O conteúdo de moléculas em combustíveis sólidos que se decompõem prontamente quando aquecidos também afeta a reatividade do resíduo não volátil.Primeiro, a decomposição da massa combustível ocorre principalmente na superfície externa do combustível. Com mais aquecimento, as reações pirogenéticas começam a ocorrer dentro das partículas de combustível, a pressão sobe nelas e a camada externa se quebra. Quando combustíveis com alto rendimento de voláteis são queimados, o resíduo de coque se torna poroso e tem uma superfície maior em comparação com o resíduo sólido denso.
2. O processo de combustão de compostos gasosos e coque
A combustão real do combustível começa com a ignição de substâncias voláteis. Durante o período de preparação do combustível, ocorrem reações em cadeia ramificada de oxidação de substâncias gasosas, a princípio essas reações ocorrem em baixas taxas. O calor liberado é percebido pelas superfícies do forno e é parcialmente acumulado na forma de energia de moléculas em movimento. O último leva a um aumento na taxa de reações em cadeia. A uma certa temperatura, as reações de oxidação ocorrem a tal taxa que o calor liberado cobre completamente a absorção de calor. Essa temperatura é o ponto de inflamação.
A temperatura de ignição não é constante, depende tanto das propriedades do combustível como das condições da zona de ignição, em média é de 400-600 ° C. Após a ignição da mistura gasosa, uma maior auto-aceleração das reações de oxidação causa um aumento da temperatura. Para manter a combustão, é necessário um suprimento contínuo de substâncias oxidantes e combustíveis.
A ignição de substâncias gasosas leva ao envolvimento da partícula de coque em um envelope de fogo. A combustão do coque começa quando a combustão dos voláteis termina. A partícula sólida aquece até uma alta temperatura e, conforme a quantidade de voláteis diminui, a espessura da camada de queima de limite diminui, o oxigênio atinge a superfície quente do carbono.
A combustão do coque começa a uma temperatura de 1000 ° C e é o processo mais longo. A razão é que, em primeiro lugar, a concentração de oxigênio diminui e, em segundo lugar, as reações heterogêneas ocorrem mais lentamente do que as homogêneas. Como resultado, a duração da combustão de uma partícula de combustível sólido é determinada principalmente pelo tempo de combustão do resíduo de coque (cerca de 2/3 do tempo total). Para combustíveis com alto rendimento de voláteis, o resíduo sólido é menor que ½ da massa inicial da partícula, portanto, sua combustão ocorre rapidamente e a possibilidade de subqueima é baixa. Os combustíveis quimicamente antigos têm uma partícula densa, cuja combustão leva quase todo o tempo gasto no forno.
O resíduo de coque da maioria dos combustíveis sólidos é principalmente, e para algumas espécies, inteiramente composto de carbono. A combustão do carbono sólido ocorre com a formação de monóxido de carbono e dióxido de carbono.
Condições ideais para dissipação de calor
A criação de condições ótimas para a combustão do carbono é a base para a correta construção de um método tecnológico de queima de combustíveis sólidos em caldeiras. Os seguintes fatores podem influenciar a obtenção da maior liberação de calor no forno: temperatura, excesso de ar, formação de mistura primária e secundária.
Temperatura... A liberação de calor durante a combustão do combustível depende significativamente do regime de temperatura do forno. Em temperaturas relativamente baixas, a combustão incompleta de substâncias combustíveis ocorre no núcleo da tocha; monóxido de carbono, hidrogênio e hidrocarbonetos permanecem nos produtos de combustão. Em temperaturas de 1000 a 1800-2000 ° C, a combustão completa do combustível é possível.
Excesso de ar... A geração de calor específico atinge seu valor máximo com combustão completa e uma relação de excesso de ar de unidade. Com a diminuição da razão de excesso de ar, a liberação de calor diminui, pois a falta de oxigênio leva à oxidação de menos combustível. O nível de temperatura diminui, as taxas de reação diminuem, o que leva a uma diminuição acentuada na liberação de calor.
Um aumento na proporção de excesso de ar maior que um reduz a geração de calor ainda mais do que a falta de ar.Em condições reais de combustão de combustível em fornos de caldeira, os valores limites de liberação de calor não são atingidos, pois ocorre combustão incompleta. Depende muito de como os processos de formação da mistura são organizados.
Processos de mistura... Em fornos de câmara, a mistura primária é obtida através da secagem e mistura de combustível com ar, fornecendo parte do ar (primário) para a zona de preparação, criando uma tocha aberta com uma superfície ampla e alta turbulência, usando ar aquecido.
Em fornos em camadas, a principal tarefa de mistura é fornecer a quantidade necessária de ar para diferentes zonas de combustão na grelha.
Para garantir a pós-combustão de produtos gasosos de combustão incompleta e coque, são organizados processos de formação de misturas secundárias. Esses processos são facilitados por: o fornecimento de ar secundário em alta velocidade, a criação de tal aerodinâmica, em que se consegue o enchimento uniforme de todo o forno com uma tocha e, conseqüentemente, o tempo de residência dos gases e partículas de coque no forno aumenta.
3. Formação de escória
No processo de oxidação da massa combustível do combustível sólido, também ocorrem mudanças significativas nas impurezas minerais. Substâncias de baixo ponto de fusão e ligas com baixo ponto de fusão dissolvem compostos refratários.
Um pré-requisito para o funcionamento normal das caldeiras é a remoção ininterrupta dos produtos da combustão e da escória resultante.
Durante a combustão da camada, a formação de escória pode levar à subqueima mecânica - impurezas minerais envolvem as partículas de coque não queimado, ou a escória viscosa pode bloquear as passagens de ar, bloqueando o acesso do oxigênio ao coque em combustão. Para reduzir a subqueima, várias medidas são usadas - em fornos com grades de corrente, o tempo gasto na grade de escória é aumentado e é realizada shuraing frequente.
Nos fornos em camadas, a escória é removida na forma seca. Em fornos de câmara, a remoção de escória pode ser seca ou líquida.
Assim, a combustão de combustíveis é um processo físico-químico complexo, que é influenciado por um grande número de fatores diferentes, mas todos eles devem ser levados em consideração no projeto de caldeiras e fornos.
Combustão - gasolina
A combustão da gasolina com detonação é acompanhada pelo aparecimento de batidas de metal cortantes, fumaça preta no escapamento, aumento do consumo de gasolina, diminuição da potência do motor e outros fenômenos negativos.
A combustão da gasolina no motor também depende da proporção do excesso de ar. Nos valores a 0 9 - j - 1 1, a taxa de processos de oxidação pré-chama na mistura de trabalho é a mais alta. Portanto, nesses valores de a, as condições mais favoráveis são criadas para o início da detonação.
Após a combustão da gasolina, a massa total desses poluentes aumentou significativamente junto com a redistribuição geral de suas quantidades. A porcentagem de benzeno no condensado dos gases de exaustão dos automóveis era cerca de 1 a 7 vezes maior do que na gasolina; o teor de tolueno era 3 vezes maior e o teor de xileno era 30 vezes maior. Sabe-se que neste caso se formam compostos de oxigênio, e o número de íons, característico dos compostos insaturados mais pesados da série das olefinas ou cicloparafinas e das séries do acetileno ou dieno, especialmente a última, aumenta drasticamente. De um modo geral, as mudanças na câmara Haagen-Smit se assemelham às mudanças necessárias para tornar a composição das amostras típicas de escapamento de veículos semelhantes às da amostra de smog de Los Angeles.
O poder calorífico da gasolina depende de sua composição química. Portanto, os hidrocarbonetos ricos em hidrogênio (por exemplo, os parafínicos) apresentam grande massa térmica de combustão.
Os produtos da combustão da gasolina se expandem no motor de combustão interna ao longo do polytrope n1 27 de 30 para 3 at. A temperatura inicial dos gases é 2100 C; a composição da massa dos produtos de combustão de 1 kg de gasolina é a seguinte: CO23 135 kg, H2 1 305 kg, O20 34 kg, N2 12 61 kg.Determine o trabalho de expansão desses gases, se 2 g de gasolina forem alimentados no cilindro ao mesmo tempo.
| Influência do TPP na formação de carbono no motor. |
Quando a gasolina é queimada em uma usina térmica, depósitos de carbono são formados contendo óxido de chumbo.
Quando a gasolina é queimada em motores alternativos de combustão interna, quase todos os produtos formados são transportados com os gases de escapamento. Apenas uma parte relativamente pequena dos produtos da combustão incompleta de combustível e óleo, uma pequena quantidade de compostos inorgânicos formados a partir de elementos introduzidos com combustível, ar e óleo, são depositados na forma de depósitos de carbono.
Quando a gasolina queima com chumbo tetraetila, aparentemente se forma óxido de chumbo, que só derrete a uma temperatura de 900 C e pode evaporar a uma temperatura muito alta, ultrapassando a temperatura média no cilindro do motor. Para evitar a deposição de óxido de chumbo no motor, substâncias especiais são introduzidas no fluido de etila - eliminadores. Os hidrocarbonetos halogenados são usados como necrófagos. Normalmente, esses compostos contêm bromo e cloro, que também queimam e ligam o chumbo em novos compostos de brometo e cloreto.
| Influência do TPP na formação de carbono no motor. |
Quando a gasolina é queimada em uma usina térmica, depósitos de carbono são formados contendo óxido de chumbo.
Durante a combustão da gasolina contendo TPP puro, uma placa de compostos de chumbo é depositada no motor. A composição do etil líquido grau R-9 (em peso): tetraetil chumbo 54 0%, bromoetano 33 0%, monocloronaftaleno 6 8 0 5%, enchimento - aviação - gasolina - até 100%; tingir vermelho escuro 1 g por 1 kg da mistura.
Quando a gasolina contendo TPP é queimada, óxido de fístula com baixa volatilidade é formado no motor; Como o ponto de fusão do óxido de chumbo é bastante elevado (888), parte dele (cerca de 10%, contando com o chumbo introduzido na gasolina) é depositado como resíduo sólido nas paredes da câmara de combustão, velas e válvulas, o que leva a uma falha rápida do motor.
Quando a gasolina é queimada no motor de um carro, moléculas menores também são formadas e a energia liberada é distribuída em um volume maior.
Os gases incandescentes da combustão da gasolina fluem em torno do trocador de calor 8 (dentro do lado da câmara de combustão e, além disso, através das janelas 5 externas, passando pela câmara de gás de exaustão 6) e aquecem o ar no canal do trocador de calor. Em seguida, os gases de escape quentes são alimentados através do tubo de escape 7 sob o reservatório e aquecem o motor do lado de fora, e o ar quente do trocador de calor é alimentado através do respiro para o cárter e aquece o motor do lado de dentro. Em 1 5 - 2 minutos após o início do aquecimento, a vela de incandescência é desligada e a combustão no aquecedor continua sem a sua participação. Após 7 - 13 minutos a partir do momento de receber um pulso para ligar o motor, o óleo no cárter aquece até uma temperatura de 30 C (a uma temperatura ambiente de até -25 C) e os pulsos de inicialização da unidade são fornecido, após o qual o aquecedor é desligado.
Temperatura de combustão
Na engenharia térmica, as seguintes temperaturas de combustão dos gases são diferenciadas: produção de calor, calorimétrica, teórica e real (calculada). A capacidade de aquecimento tx é a temperatura máxima dos produtos da combustão completa do gás em condições adiabáticas com um coeficiente de excesso de ar a = 1,0 e a uma temperatura do gás e do ar igual a 0 ° C:
tx = Qh / (IVcv) (8.11)
onde QH é o valor calorífico mais baixo do gás, kJ / m3; IVcp - a soma dos produtos dos volumes de dióxido de carbono, vapor d'água e nitrogênio formados durante a combustão de 1 m3 de gás (m3 / m3) e suas capacidades térmicas volumétricas médias a pressão constante na faixa de temperatura de 0 ° С tx (kJ / (m3 * ° С).
Devido à inconstância da capacidade calorífica dos gases, a produção de calor é determinada pelo método de aproximações sucessivas. Como parâmetro inicial toma-se o seu valor para o gás natural (= 2000 ° C), com a = 1,0, são determinados os volumes dos componentes dos produtos da combustão, conforme tabela.8.3, sua capacidade térmica média é encontrada e, a seguir, de acordo com a fórmula (8.11), a capacidade térmica do gás é calculada. Se, como resultado do cálculo, for menor ou maior do que o aceito, então uma temperatura diferente é definida e o cálculo é repetido. A produção de calor de gases comuns simples e complexos quando eles queimam no ar seco é fornecida na tabela. 8,5. Ao queimar gás no ar atmosférico contendo cerca de 1 peso % de umidade, a produção de calor diminui em 25-30 ° С.
A temperatura calorimétrica de combustão tK é a temperatura determinada sem levar em conta a dissociação do vapor d'água e do dióxido de carbono, mas levando em consideração a temperatura inicial real do gás e do ar. Ele difere da saída de calor tx porque as temperaturas do gás e do ar, bem como o excesso do coeficiente de ar a, são retirados de seus valores reais. Você pode determinar tK pela fórmula:
tк = (Qн + qphys) / (ΣVcp) (8.12)
onde qphys é o conteúdo de calor (calor físico) do gás e do ar, medido a partir de 0 ° C, kJ / m3.
Os gases de petróleo naturais e liquefeitos geralmente não são aquecidos antes da combustão e seu volume em comparação com o volume do ar de combustão é pequeno.
Tabela 8.3.
Capacidade média de calor volumétrico dos gases, kJ / (m3 • ° С)
| Ttemperatura, ° С | CO2 | N2 | O2 | CO | CH4 | H2 | H2O (vapor d'água) | ar | |
| seco | úmido por m3 de gás seco mas | ||||||||
| 0 | 1,5981 | 1,2970 | 1,3087 | 1,3062 | 1,5708 | 1,2852 | 1,4990 | 1,2991 | 1,3230 |
| 100 | 1,7186 | 1,2991 | 1,3209 | 1,3062 | 1,6590 | 1,2978 | 1,5103 | 1,3045 | 1,3285 |
| 200 | 1,8018 | 1,3045 | 1,3398 | 1,3146 | 1,7724 | 1,3020 | 1,5267 | 1,3142 | 1,3360 |
| 300 | 1,8770 | 1,3112 | 1,3608 | 1,3230 | 1,8984 | 1,3062 | 1,5473 | 1,3217 | 1,3465 |
| 400 | 1,9858 | 1,3213 | 1,3822 | 1,3356 | 2,0286 | 1,3104 | 1,5704 | 1,3335 | 1,3587 |
| 500 | 2,0030 | 1,3327 | 1,4024 | 1,3482 | 2,1504 | 1,3104 | 1,5943 | 1,3469 | 1,3787 |
| 600 | 2,0559 | 1,3453 | 1,4217 | 1,3650 | 2,2764 | 1,3146 | 1,6195 | 1,3612 | 1,3873 |
| 700 | 2,1034 | 1,3587 | 1,3549 | 1,3776 | 2,3898 | 1,3188 | 1,6464 | 1,3755 | 1,4020 |
| 800 | 2,1462 | 1,3717 | 1,4549 | 1,3944 | 2,5032 | 1,3230 | 1,6737 | 1,3889 | 1,4158 |
| 900 | 2,1857 | 1,3857 | 1,4692 | 1,4070 | 2,6040 | 1,3314 | 1,7010 | 1,4020 | 1,4293 |
| 1000 | 2,2210 | 1,3965 | 1,4822 | 1,4196 | 2,7048 | 1,3356 | 1,7283 | 1,4141 | 1,4419 |
| 1100 | 2,2525 | 1,4087 | 1,4902 | 1,4322 | 2,7930 | 1,3398 | 1,7556 | 1,4263 | 1,4545 |
| 1200 | 2,2819 | 1,4196 | 1,5063 | 1,4448 | 2,8812 | 1,3482 | 1,7825 | 1,4372 | 1,4658 |
| 1300 | 2,3079 | 1,4305 | 1,5154 | 1,4532 | — | 1,3566 | 1,8085 | 1,4482 | 1,4771 |
| 1400 | 2,3323 | 1,4406 | 1,5250 | 1,4658 | — | 1,3650 | 1,8341 | 1,4582 | 1,4876 |
| 1500 | 2,3545 | 1,4503 | 1,5343 | 1,4742 | — | 1,3818 | 1,8585 | 1,4675 | 1,4973 |
| 1600 | 2,3751 | 1,4587 | 1,5427 | — | — | — | 1,8824 | 1,4763 | 1,5065 |
| 1700 | 2,3944 | 1,4671 | 1,5511 | — | — | — | 1,9055 | 1,4843 | 1,5149 |
| 1800 | 2,4125 | 1,4746 | 1,5590 | — | — | — | 1,9278 | 1,4918 | 1,5225 |
| 1900 | 2,4289 | 1,4822 | 1,5666 | — | — | — | 1,9698 | 1,4994 | 1,5305 |
| 2000 | 2,4494 | 1,4889 | 1,5737 | 1,5078 | — | — | 1,9694 | 1,5376 | 1,5376 |
| 2100 | 2,4591 | 1,4952 | 1,5809 | — | — | — | 1,9891 | — | — |
| 2200 | 2,4725 | 1,5011 | 1,5943 | — | — | — | 2,0252 | — | — |
| 2300 | 2,4860 | 1,5070 | 1,5943 | — | — | — | 2,0252 | — | — |
| 2400 | 2,4977 | 1,5166 | 1,6002 | — | — | — | 2,0389 | — | — |
| 2500 | 2,5091 | 1,5175 | 1,6045 | — | — | — | 2,0593 | — | — |
Portanto, ao determinar a temperatura calorimétrica, o conteúdo de calor dos gases pode ser ignorado. Na queima de gases de baixo valor calorífico (gerador, alto-forno, etc.), seu conteúdo de calor (especialmente aquecido antes da combustão) tem um efeito muito significativo na temperatura calorimétrica.
A dependência da temperatura calorimétrica do gás natural de composição média no ar com uma temperatura de 0 ° C e uma umidade de 1% sobre o excesso de coeficiente de ar a é dada na Tabela. 8.5, para o GLP quando é queimado em ar seco - em mesa. 8,7. Dados da tabela. 8.5-8.7 é possível ser orientado com precisão suficiente ao estabelecer a temperatura calorimétrica de combustão de outros gases naturais, que são relativamente semelhantes em composição, e gases de hidrocarbonetos de quase qualquer composição. Se for necessário obter alta temperatura na queima de gases com baixos coeficientes de excesso de ar, bem como aumentar a eficiência dos fornos, na prática, o ar é aquecido, o que leva a um aumento da temperatura calorimétrica (ver Tabela 8.6) .
Tabela 8.4.
Capacidade de aquecimento de gases em ar seco
| Gás simples | Capacidade de aquecimento, ° С | Gás complexo de composição média | Produção de calor aproximada, ° С |
| Hidrogênio | 2235 | Campos de gás natural | 2040 |
| Monóxido de carbono | 2370 | Campos de óleo natural | 2080 |
| Metano | 2043 | Coca | 2120 |
| Etano | 2097 | Destilação de xisto em alta temperatura | 1980 |
| Propano | 2110 | Explosão de vapor de oxigênio sob pressão | 2050 |
| Butano | 2118 | Gerador de carvão gordo | 1750 |
| Pentano | 2119 | Explosão de vapor-ar do gerador de combustíveis pobres | 1670 |
| Etileno | 2284 | Liquefeito (50% C3H4 + 50% C4H10) | 2115 |
| Acetileno | 2620 | Água | 2210 |
Tabela 8.5.
Temperaturas calorimétricas e teóricas de combustão do gás natural no ar com t = 0 ° С e umidade 1% * dependendo do excesso de coeficiente de ar a
| Proporção de excesso de ar a | Calorimétrico temperatura de combustão tк, ° С | Teórico temperatura de combustão | Proporção de excesso de ar a | Calorimétrico temperatura de combustão tк, ° С |
| 1,0 | 2010 | 1920 | 1,33 | 1620 |
| 1,02 | 1990 | 1900 | 1,36 | 1600 |
| 1,03 | 1970 | 1880 | 1,40 | 1570 |
| 1,05 | 1940 | 1870 | 1,43 | 1540 |
| 1,06 | 1920 | 1860 | 1,46 | 1510 |
| 1,08 | 1900 | 1850 | 1,50 | 1470 |
| 1,10 | 1880 | 1840 | 1,53 | 1440 |
| 1,12 | 1850 | 1820 | 1,57 | 1410 |
| 1,14 | 1820 | 1790 | 1,61 | 1380 |
| 1,16 | 1800 | 1770 | 1,66 | 1350 |
| 1,18 | 1780 | 1760 | 1,71 | 1320 |
| 1,20 | 1760 | 1750 | 1,76 | 1290 |
| 1,22 | 1730 | — | 1,82 | 1260 |
| 1,25 | 1700 | — | 1,87 | 1230 |
| 1,28 | 1670 | — | 1,94 | 1200 |
| 1,30 | 1650 | — | 2,00 | 1170 |
>
A temperatura teórica de combustão tT é a temperatura máxima determinada de forma semelhante à temperatura calorimétrica tK, mas com uma correção para reações endotérmicas (requerendo calor) de dissociação de dióxido de carbono e vapor de água, procedendo com aumento de volume:
СО2 ‹–› СО + 0,5О2 - 283 mJ / mol (8,13)
Н2О ‹–› Н2 + 0,5О2 - 242 mJ / mol (8.14)
Em altas temperaturas, a dissociação pode levar à formação de hidrogênio atômico, oxigênio e grupos hidroxila OH. Além disso, quando o gás é queimado, algum óxido de nitrogênio sempre é gerado. Todas essas reações são endotérmicas e levam à diminuição da temperatura de combustão.
Tabela 8.6.
Temperatura calorimétrica de combustão do gás natural tу, ° С, dependendo da relação entre o excesso de ar seco e sua temperatura (valores arredondados)
| Proporção de excesso de ar a | Temperatura do ar seco, ° С | ||||||||
| 20 | 100 | 200 | 300 | 400 | 500 | 600 | 700 | 800 | |
| 0,5 | 1380 | 1430 | 1500 | 1545 | 1680 | 1680 | 1740 | 1810 | 1860 |
| 0,6 | 1610 | 1650 | 1715 | 1780 | 1840 | 1900 | 1960 | 2015 | 2150 |
| 0,7 | 1730 | 1780 | 1840 | 1915 | 1970 | 2040 | 2100 | 2200 | 2250 |
| 0,8 | 1880 | 1940 | 2010 | 2060 | 2130 | 2200 | 2260 | 2330 | 2390 |
| 0,9 | 1980 | 2030 | 2090 | 2150 | 2220 | 2290 | 2360 | 2420 | 2500 |
| 1,0 | 2050 | 2120 | 2200 | 2250 | 2320 | 2385 | 2450 | 2510 | 2560 |
| 1,2 | 1810 | 1860 | 1930 | 2000 | 2070 | 2140 | 2200 | 2280 | 2350 |
| 1,4 | 1610 | 1660 | 1740 | 1800 | 2870 | 1950 | 2030 | 2100 | 2160 |
| 1,6 | 1450 | 1510 | 1560 | 1640 | 1730 | 1800 | 1860 | 1950 | 2030 |
| 1,8 | 1320 | 1370 | 1460 | 1520 | 1590 | 1670 | 1740 | 1830 | 1920 |
| 2,0 | 1220 | 1270 | 1360 | 1420 | 1490 | 1570 | 1640 | 1720 | 1820 |
Tabela 8.7.
Temperatura de combustão calorimétrica tK do propano comercial em ar seco com t = 0 ° С dependendo do excesso de coeficiente de ar a
| Proporção de excesso de ar a | Temperatura de combustão calorimétrica tH, ° С | Proporção de excesso de ar a | Temperatura de combustão calorimétrica tK, ° С |
| 1,0 | 2110 | 1,45 | 1580 |
| 1,02 | 2080 | 1,48 | 1560 |
| 1,04 | 2050 | 1,50 | 1540 |
| 1,05 | 2030 | 1,55 | 1500 |
| 1,07 | 2010 | 1,60 | 1470 |
| 1,10 | 1970 | 1,65 | 1430 |
| 1,12 | 1950 | 1,70 | 1390 |
| 1,15 | 1910 | 1,75 | 1360 |
| 1,20 | 1840 | 1,80 | 1340 |
| 1,25 | 1780 | 1,85 | 1300 |
| 1,27 | 1750 | 1,90 | 1270 |
| 1,30 | 1730 | 1,95 | 1240 |
| 1,35 | 1670 | 2,00 | 1210 |
| 1,40 | 1630 | 2,10 | 1170 |
A temperatura de combustão teórica pode ser determinada usando a seguinte fórmula:
tT = (Qн + qphys - qdis) / (ΣVcp) (8.15)
onde qduc é o consumo total de calor para a dissociação de СО2 e Н2О em produtos de combustão, kJ / m3; IVcp - a soma do produto do volume e da capacidade térmica média dos produtos da combustão, levando em consideração a dissociação por 1 m3 de gás.
Como você pode ver na tabela. 8.8, em temperaturas de até 1600 ° C, o grau de dissociação pode ser desconsiderado e a temperatura teórica de combustão pode ser considerada igual à temperatura calorimétrica. Em temperaturas mais altas, o grau de dissociação pode reduzir significativamente a temperatura na área de trabalho. Na prática, isso não é necessário, a temperatura teórica de combustão deve ser determinada apenas para fornos de alta temperatura operando com ar pré-aquecido (por exemplo, fornos de lareira). Isso não é necessário para as caldeiras.
A temperatura real (calculada) dos produtos de combustão td é a temperatura que é atingida em condições reais no ponto mais quente da chama. É inferior ao teórico e depende da perda de calor para o ambiente, do grau de transferência de calor da zona de combustão por radiação, da duração do processo de combustão no tempo, etc. da temperatura nos fornos com a introdução de fatores de correção experimentalmente estabelecidos para eles:
td = t (8,16)
onde n - t. n. coeficiente pirométrico dentro de:
- para fornos térmicos e de aquecimento de alta qualidade com isolamento térmico - 0,75-0,85;
- para fornos selados sem isolamento térmico - 0,70-0,75;
- para fornos de caldeira blindados - 0,60-0,75.
Na prática, é necessário conhecer não apenas as temperaturas de combustão adiabática fornecidas acima, mas também as temperaturas máximas que ocorrem na chama. Seus valores aproximados são geralmente estabelecidos experimentalmente por métodos espectrográficos. As temperaturas máximas que surgem em uma chama livre a uma distância de 5-10 mm do topo da frente cônica de combustão são fornecidas na tabela. 8,9. Uma análise dos dados apresentados mostra que as temperaturas máximas na chama são menores que a saída de calor (devido ao consumo de calor para a dissociação de H2O e CO2 e a retirada de calor da zona da chama).
- casa
- Diretório
- Características de combustão de gases
- Temperatura de combustão
Combustão - produto de óleo
A combustão de derivados de petróleo no aterro da área de tanques é eliminada pelo fornecimento imediato de espuma.
A combustão de derivados de petróleo no aterro da área de tanques é eliminada pelo fornecimento imediato de espuma.
Durante a combustão de produtos petrolíferos, seu ponto de ebulição (ver Tabela 69) aumenta gradualmente devido à destilação fracionada em curso, em conexão com a qual a temperatura da camada superior também aumenta.
| K Diagrama de um sistema de abastecimento de água de combate a incêndio para resfriar um tanque em chamas através de um anel de irrigação. |
Ao queimar óleo no tanque, a parte superior da correia superior do tanque fica exposta à chama. Ao queimar óleo em um nível inferior, a altura do lado livre do tanque em contato com a chama pode ser significativa. Neste modo de combustão, o reservatório pode entrar em colapso. Água de bicos de incêndio ou de anéis de irrigação estacionários, caindo na parte externa das paredes superiores do tanque, os resfria (Fig.15.1), evitando assim um acidente e espalhamento de óleo no aterro, criando condições mais favoráveis para o uso de espuma aeromecânica.
Os resultados do estudo da combustão de derivados de petróleo e suas misturas são interessantes.
Sua temperatura durante a combustão de derivados de petróleo é: gasolina 1200 C, querosene de trator 1100 C, óleo diesel 1100 C, óleo cru 1100 C, óleo combustível 1000 C. Ao queimar madeira em pilhas, a temperatura da chama turbulenta chega a 1200 - 1300 C.
Particularmente grandes estudos no campo da física da combustão de produtos petrolíferos e sua extinção foram realizados nos últimos 15 anos no Instituto Central de Pesquisa de Defesa contra Incêndio (TsNIIPO), no Instituto de Energia da Academia de Ciências da URSS (ENIN) e uma série de outros institutos de pesquisa e educação.
Um exemplo de catálise negativa é a supressão da combustão de derivados de petróleo com adição de hidrocarbonetos halogenados.
A água promove a formação de espuma e emulsões durante a combustão de derivados de petróleo com um ponto de fulgor de 120 C e superior. A emulsão, que cobre a superfície do líquido, isola-o do oxigênio do ar e também impede a saída de seus vapores.
| Taxa de combustão de gases de hidrocarbonetos liquefeitos em tanques isotérmicos. |
A combustão de gases de hidrocarbonetos liquefeitos em tanques isotérmicos não difere da combustão de produtos petrolíferos. A taxa de combustão, neste caso, pode ser calculada pela fórmula (13) ou determinada experimentalmente. A peculiaridade da combustão de gases liquefeitos em condições isotérmicas é que a temperatura de toda a massa de líquido no tanque é igual ao ponto de ebulição à pressão atmosférica. Para hidrogênio, metano, etano, propano e butano, essas temperaturas são, respectivamente, - 252, - 161, - 88, - 42 e 0 5 C.
| Esquema de instalação do gerador GVPS-2000 no tanque. |
A pesquisa e a prática de extinção de incêndios têm demonstrado que, para interromper a combustão de um produto petrolífero, a espuma deve cobrir completamente toda a sua superfície com uma camada de certa espessura. Todas as espumas com baixa taxa de expansão são ineficazes na extinção de incêndios de derivados de petróleo em tanques com nível inferior de inundação. A espuma, caindo de uma grande altura (6 - 8 m) na superfície do combustível, é mergulhada e envolvida em uma película de combustível, queima ou desmorona rapidamente. Somente espuma com uma multiplicidade de 70 - 150 pode ser lançada em um tanque em chamas com jatos articulados.
| Quebra-fogo. |